17.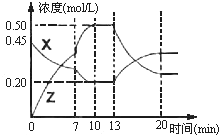 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )
 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中X、Z的物质的量浓度随时间变化的曲线.根据以上信息判断,下列说法中正确的是( )| A. | 化学方程式中a:b=1:3 | |
| B. | 推测在第7min时曲线变化的原因可能是升温 | |
| C. | 推测在第13min时该反应刚好达到化学平衡 | |
| D. | 用X表示O~10min内该反应的平均速率为v(X)=0.045mol•L-1•mol-1 |
16.下列除杂的操作不正确的是( )
| A. | MgCl2溶液中混有少量FeCl3:加入足量镁充分反应后过滤 | |
| B. | FeCl2溶液中混有少量FeCl3:加入足量铁粉充分反应后过滤 | |
| C. | CuCl2溶液中混有少量FeCl3:加入NaOH溶液充分反应后过滤 | |
| D. | CuCl2溶液中混有少量FeCl2:先加入H2O2将Fe2+氧化成Fe3+,再加入CuO充分反应后过滤 |
14.在密闭容器中进行反应:X(g)+4Y(g)?2Z(g)+3W(g),其中X、Y、Z、W的起始浓度分别为0.1mol•L-1、0.4mol•L-1、0.2mol•L-1、0.3mol•L-1,在一定条件下,当反应达到平衡时,各物质的浓度不可能是( )
| A. | c(X)=0.15mol•L-1 | B. | c(Y)=0.9mol•L-1 | C. | c(Z)=0.3mol•L-1 | D. | c(W)=0.6mol•L-1 |
11.已知Fe5O7可以看作Fe2O3和Fe3O4的混合物.现有Fe、Fe5O7混合物共0.1mol,加盐酸后固体全部溶解,共收集到0.01mol H2,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中铁的物质的量为( )
| A. | 0.05mol | B. | 0.06mol | C. | 0.07mol | D. | 0.08mol |
9.下列有关电化学的说法不正确的是( )
| A. | Zn具有还原性和导电性,可用作锌锰干电池的负极材料 | |
| B. | 锂碘电池的总反应为2Li(s)+I2(s)═2LiI(s),则碘电极作该电池的负极 | |
| C. | 铅蓄电池放电时的负极和充电时的阳极均发生氧化反应 | |
| D. | 锌与稀硫酸反应时,要加大反应速率,可滴加少量硫酸铜 |
8.下列离子方程式正确的是( )
0 171543 171551 171557 171561 171567 171569 171573 171579 171581 171587 171593 171597 171599 171603 171609 171611 171617 171621 171623 171627 171629 171633 171635 171637 171638 171639 171641 171642 171643 171645 171647 171651 171653 171657 171659 171663 171669 171671 171677 171681 171683 171687 171693 171699 171701 171707 171711 171713 171719 171723 171729 171737 203614
| A. | NaHCO3与HCl的反应:HCO3-+H+=CO2↑H2O | |
| B. | 盐酸跟氢氧化镁反应:H++OH-=H2O | |
| C. | Cu与AgNO3的反应:Cu+Ag+=Cu2++Ag | |
| D. | Fe与H2SO4的反应:2Fe+6H+=2Fe3++3H2↑ |
 室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示.
室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示.