10.下列说法不正确的是( )
| A. | 0.2 mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) | |
| B. | 叠氮酸(HN3)与醋酸相似,NaN3水溶液中离子浓度大小为c(Na+)>c(N3-)>c(OH-)>c(H+)[ | |
| C. | 向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中c(NH4+)=c(Cl-) | |
| D. | 常温下,pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7 |
9.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 78g苯含有C=C双键的数目为3NA | |
| B. | 1L 0.1mol/L的NaClO溶液中含有ClO-的数目为0.1NA | |
| C. | 常温常压下,14g由N2和CO组成的混合气体含有的原子数为NA | |
| D. | 标准状况下,6.72L NO2与水反应转移电子数为0.1NA |
7.将50mL某AlCl3溶液加入30mL 1mol/L NaOH溶液或50mL 1.8mol/L NaOH溶液中,均能得到0.78g白色沉淀.则此AlCl3溶液的浓度是( )
| A. | 0.5 mol/L | B. | 0.4 mol/L | C. | 0.3 mol/L | D. | 0.2 mol/L |
6.在实验室配制0.10mol•L-1的KCl溶液,下列操作会导致所配溶液浓度偏高的是( )
| A. | 转移溶液时使用的烧杯未洗涤 | B. | 定容时俯视读取刻度线 | ||
| C. | 原容量瓶洗净后未干燥 | D. | 转移时有少量溶液流出瓶外 |
5.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向无色溶液中滴加氯水和CCl4,振荡静置 | 下层溶液显 紫色 | 原溶液中含有I- |
| B | 过量铁粉加入稀硝酸中充分反应,再加入KSCN溶液 | 溶液呈红色 | 稀硝酸将铁 氧化为Fe2+ |
| C | 向淀粉溶液中滴加稀硫酸,加热,取水解液少许,滴加银氨溶液,并水浴加热 | 没有银镜出现 | 淀粉没有发生水解 |
| D | 用玻璃棒蘸取浓硫酸滴到蓝色石蕊试纸上 | 试纸变黑 | 浓硫酸具有脱水性 |
| A. | A | B. | B | C. | C | D. | D |
4. 反应2NO2(g)?N2O4(g)△H=-57kJ/mol,若保持气体总质量不变.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应2NO2(g)?N2O4(g)△H=-57kJ/mol,若保持气体总质量不变.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
 反应2NO2(g)?N2O4(g)△H=-57kJ/mol,若保持气体总质量不变.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应2NO2(g)?N2O4(g)△H=-57kJ/mol,若保持气体总质量不变.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A. | a、c两点气体的颜色:a浅,c深 | |
| B. | a、c两点气体的平均相对分子质量:a>c | |
| C. | b、c两点的平衡常数:Kb=Kc | |
| D. | 状态a通过升高温度可变成状态b |
3.在催化剂、400℃时可实现氯的循环利用,如图是其能量关系图,下列分析正确的是( )
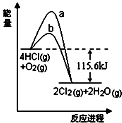

| A. | 曲线a是使用了催化剂的能量变化曲线 | |
| B. | 反应物的总键能高于生成物的总键能 | |
| C. | 反应的热化学方程式为:4HCl(g)+O2(g)$→_{400℃}^{催化剂}$2Cl2+2H2O(g)△H=+115.6 kJ/mol | |
| D. | 若反应生成2 mol 液态水,放出的热量高于115.6 kJ |
2.下列工业生产过程中涉及不到氧化还原反应的是( )
0 171500 171508 171514 171518 171524 171526 171530 171536 171538 171544 171550 171554 171556 171560 171566 171568 171574 171578 171580 171584 171586 171590 171592 171594 171595 171596 171598 171599 171600 171602 171604 171608 171610 171614 171616 171620 171626 171628 171634 171638 171640 171644 171650 171656 171658 171664 171668 171670 171676 171680 171686 171694 203614
| A. | 接触法制硫酸 | B. | 侯德榜制纯碱 | ||
| C. | 粗铜精炼 | D. | 石油的裂化和裂解 |
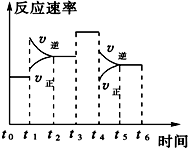 (1)25℃时,合成氨反应的热化学方程式为:N2(g)+3H2(g)2NH3(g)△H=-92.4kJ/mol 反应过程如图.
(1)25℃时,合成氨反应的热化学方程式为:N2(g)+3H2(g)2NH3(g)△H=-92.4kJ/mol 反应过程如图.