19.下列叙述不正确的是( )
| A. | 不锈钢是化合物 | |
| B. | 合金的硬度一般比它的各成分金属的硬度大 | |
| C. | 黄铜是混合物 | |
| D. | 合金的熔点一般比它的各成分金属的熔点低 |
17.下列各组物质中化学键的类型相同的是( )
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O ? CO2 | ||
| C. | NH3 H2O CO2 | D. | CaCl2 ? NaOH H2O |
16.元素的性质随着元素原子序数的递增而呈周期性变化的根本原因是( )
| A. | 元素原子的核外电子排布的周期性变化 | |
| B. | 元素的相对原子质量逐渐增大 | |
| C. | 元素化合价的周期性变化 | |
| D. | 元素原子的核外电子层数的逐渐增多 |
15.在不同条件下分别测得反应2SO2+O2?2SO3的化学反应速率,其中表示该反应进行得最快的是( )
| A. | v(SO2)=4 mol/(L•min) | B. | v(O2)=3 mol/(L•min) | ||
| C. | v(SO3)=6 mol/(L•min) | D. | v(O2)=6 mol/(L•min) |
13.对于A2+3B2═2C+D的反应来说,以下化学反应速率的表示中,反应速率最快的为( )
| A. | V(B2)=0.8mol/( L•s) | B. | V(A2)=0.8mol/( L•min) | ||
| C. | V(C)=0.6mol/( L•s) | D. | V(D)=0.8mol/( L•s) |
11.对于锌、铜和稀硫酸组成的原电池,下列有关说法正确的是( )
| A. | Zn是正极 | B. | 电子由铜片经外电路流向锌片 | ||
| C. | Zn-2e-═Zn2+ | D. | 溶液中H+向锌片迁移 |
10.氮是地球上含量丰富的一种元素,氮及其化合物在生产生活中有着重要作用.
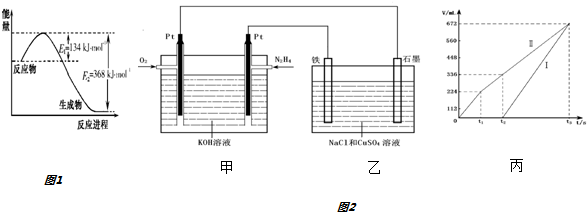
(1)如图1是1mol NO2气体和1mol CO反应生成CO2和NO过程中能量变化示意图.则反应过程中放出的总热量应为234kJ.
(2)在固定体积的密闭容器中,进行如下化学反应:
N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的 关系如下表:
①写出该反应的平衡常数表达式.K=$\frac{c{\;}^{2}(NH{\;}_{3})}{c(N{\;}_{2})×c{\;}^{3}(H{\;}_{2})}$.
②试判断K1>K2(填写“>”“=”或“<”)
③下列各项能说明该反应已达到平衡状态的是c(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(N2)=3v(H2)
c.容器内压强保持不变 d.混合气体的密度保持不变
(3)化合物N2 H4 做火箭发动机的燃料时,与氧化剂N2O4反应生成N2和水蒸气.
某同学设计了一个N2H4--空气碱性燃料电池,并用该电池电解200mL一定浓度NaCl与CuSO4混合溶液,其装置如图2所示.
①该燃料电池的负极反应式为N2H4+4OH--4e-=N2↑+4H2O;
②理论上乙中两极所得气体的体积随时间变化的关系如丙图中曲线 I、II所示(气体体积已换算成标准状况下的体积),写出在t1-t2时间段铁电极上的电极反应式Cu2++2e-=Cu;原混合溶液中NaCl的物质的量浓度为0.1mol/L
③在t2时所得溶液的pH为1.(假设溶液体积不变)
0 171350 171358 171364 171368 171374 171376 171380 171386 171388 171394 171400 171404 171406 171410 171416 171418 171424 171428 171430 171434 171436 171440 171442 171444 171445 171446 171448 171449 171450 171452 171454 171458 171460 171464 171466 171470 171476 171478 171484 171488 171490 171494 171500 171506 171508 171514 171518 171520 171526 171530 171536 171544 203614
(1)如图1是1mol NO2气体和1mol CO反应生成CO2和NO过程中能量变化示意图.则反应过程中放出的总热量应为234kJ.
(2)在固定体积的密闭容器中,进行如下化学反应:
N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的 关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
②试判断K1>K2(填写“>”“=”或“<”)
③下列各项能说明该反应已达到平衡状态的是c(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(N2)=3v(H2)
c.容器内压强保持不变 d.混合气体的密度保持不变
(3)化合物N2 H4 做火箭发动机的燃料时,与氧化剂N2O4反应生成N2和水蒸气.
某同学设计了一个N2H4--空气碱性燃料电池,并用该电池电解200mL一定浓度NaCl与CuSO4混合溶液,其装置如图2所示.
①该燃料电池的负极反应式为N2H4+4OH--4e-=N2↑+4H2O;
②理论上乙中两极所得气体的体积随时间变化的关系如丙图中曲线 I、II所示(气体体积已换算成标准状况下的体积),写出在t1-t2时间段铁电极上的电极反应式Cu2++2e-=Cu;原混合溶液中NaCl的物质的量浓度为0.1mol/L
③在t2时所得溶液的pH为1.(假设溶液体积不变)

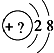 某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.
某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断. ;
;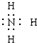 .
.