14.已知反应3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,当转移6mol电子时,被还原的HNO3的物质的量为( )
| A. | 8mol | B. | 4mol | C. | 2mol | D. | 6mol |
13.下列反应中,离子方程式书写正确的是( )
| A. | 大理石与硝酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 过量CO2与澄清石灰水反应:Ca2++2OH-+CO2═CaCO3↓+H2O | |
| C. | NH4HSO3与少量NaOH反应:NH4++HSO3-+20H-═NH3•H2O+SO32-+H2O | |
| D. | (NH4)2SO4与Ba(OH)2反应:2NH4++SO42-+Ba2++2OH-═BaSO4↓+2NH3•H2O |
12.化学知识在生产和生活中有着重要的应用.下列说法中正确的是( )
| A. | 明矾常作为消毒剂 | |
| B. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| C. | 高纯度的硅单质广泛用于制作光导纤维 | |
| D. | 钠的还原性很强,可以用来冶炼金属钛、钽、铌、锆等 |
11.下列说法中正确的是( )
| A. | 标准状况下,22.4L水中所含的分子数约为6.02×1023个 | |
| B. | 1 mol Cl2参加反应转移电子数一定为2 NA个 | |
| C. | 48gO3与O2的混合气体中含有的氧原子数为3NA 个 | |
| D. | 从1L0.5 mol/LNaCl溶液中取出100mL,剩余溶液中NaCl物质的量浓度为0.45mol/L |
10.T1温度下,反应2SO2(g)+O2(g)?2SO3(g)△H<0的平衡常数K=532.4.
(1)该反应平衡常数的表达式为K=$\frac{c{\;}^{2}(SO{\;}_{3})}{c{\;}^{2}(SO{\;}_{2})c(O{\;}_{2})}$,
T1温度下,某时刻测得体系中各物质浓度分别为c(SO2)=0.0600mol•L-1,c(O2)=0.400mol•L-1,c(SO3)=2.000mol•L-1,此时反应进行的方向为逆反应方向.
(2)该反应△S<0,升高温度,平衡常数减小(填“增大”“减小”或“不变”)
(3)T2温度下,2L容积固定的甲、乙两密闭容器中发生上述反应,测得平衡时有关数据如下:
1下列能说明T2温度下甲容器中上述反应已达到平衡状态的是AB.
A.SO2、O2、SO3的物质的量浓度之比为212
B.容器内气体压强不再变化
C.单位时间内生成2v(SO2)消耗=v(O2)生成
D.容器内混合气体的密度不再变化
②分析表格中数据,α1+α2< 1(填“>”“=”或“<”),T1<T2(填“>”“=”或“<”).
(1)该反应平衡常数的表达式为K=$\frac{c{\;}^{2}(SO{\;}_{3})}{c{\;}^{2}(SO{\;}_{2})c(O{\;}_{2})}$,
T1温度下,某时刻测得体系中各物质浓度分别为c(SO2)=0.0600mol•L-1,c(O2)=0.400mol•L-1,c(SO3)=2.000mol•L-1,此时反应进行的方向为逆反应方向.
(2)该反应△S<0,升高温度,平衡常数减小(填“增大”“减小”或“不变”)
(3)T2温度下,2L容积固定的甲、乙两密闭容器中发生上述反应,测得平衡时有关数据如下:
| 容器 | 甲 | 乙 |
| 反应物投入量 | 2molSO2、1molO2 | 4molSO3 |
| 平衡时n(SO3)/mol | 1 | m |
| 反应物的转化率 | α1 | α2 |
A.SO2、O2、SO3的物质的量浓度之比为212
B.容器内气体压强不再变化
C.单位时间内生成2v(SO2)消耗=v(O2)生成
D.容器内混合气体的密度不再变化
②分析表格中数据,α1+α2< 1(填“>”“=”或“<”),T1<T2(填“>”“=”或“<”).
9.下列说法正确的是( )
| A. | 金属甲的阳离子比同价态的金属乙的阳离子氧化性强,则金属甲比金属乙活泼 | |
| B. | 原电池中电子从负极经过溶液流向正极 | |
| C. | 电解池中电解质溶液的阳离子向阴极迁移 | |
| D. | 在铁制品上镀银,铁做正极,银做负极 |
8.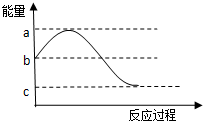 反应A(g)+3B (g)?2C(g)的能量变化如图所示,结合图象分析下列说法,其中正确的是( )
反应A(g)+3B (g)?2C(g)的能量变化如图所示,结合图象分析下列说法,其中正确的是( )
 反应A(g)+3B (g)?2C(g)的能量变化如图所示,结合图象分析下列说法,其中正确的是( )
反应A(g)+3B (g)?2C(g)的能量变化如图所示,结合图象分析下列说法,其中正确的是( )| A. | 若升高温度,则平衡常数增大 | |
| B. | 该反应的焓变为b-a | |
| C. | 达到平衡后,增大压强,平衡逆移 | |
| D. | 催化剂不影响反应的焓变,影响反应的活化能 |
7.NA代表阿伏加德罗常数,则关于热化学方程C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(l)△H=-1300kJ•mol-1的说法中,正确的是( )
| A. | 有10NA个电子转移时,放出1300kJ的能量 | |
| B. | 有44.8LCO2气体生成时,放出1300kJ的能量 | |
| C. | 有NA个水分子生成且为液体时,吸收1300kJ的能量 | |
| D. | 有4NA个碳氧共用电子对生成时,放出1300kJ的能量 |
6.下列说法正确的是( )
0 171332 171340 171346 171350 171356 171358 171362 171368 171370 171376 171382 171386 171388 171392 171398 171400 171406 171410 171412 171416 171418 171422 171424 171426 171427 171428 171430 171431 171432 171434 171436 171440 171442 171446 171448 171452 171458 171460 171466 171470 171472 171476 171482 171488 171490 171496 171500 171502 171508 171512 171518 171526 203614
| A. | 活化分子间发生的碰撞就是有效碰撞 | |
| B. | 增大反应物浓度会加快反应速率,原因是增大了活化分子百分数,从而使有效碰撞次数增加 | |
| C. | 吸热反应,升高温度,v正增大,v逆减小 | |
| D. | 有气体参与的反应达到平衡后,增大压强,平衡可能不移动 |