9.由氧化铜、氧化铁组成的混合物ag,加入2mol•L-1的硫酸50mL时固体恰好完全溶解.若将ag该混合物在足量的一氧化碳中加热充分反应,冷却后固体质量减少为( )
| A. | 1.6g | B. | (a-1.6)g | C. | (a-3.2)g | D. | 无法计算 |
8.用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 1 mol甲烷的质量与甲烷的摩尔质量相等 | |
| B. | 28 g氮气与40 g氩气所含的原子数目相等,都是NA个 | |
| C. | 2.3 g钠和过量氧气反应,失去的电子数为0.1NA | |
| D. | 18 g重水(D2O)所含的电子数为10NA |
7.金属汞在加热条件下能和氧气化合生成氧化汞,反应如下:2Hg+O2═2HgO,下列哪个选项可以说明0.4molHg 与 0.4molO2充分反应后物质的种类及其量的情况.( )
| A. | 0.1molHgO与0.3molHg | B. | 0.2molHgO与0.2mol Hg | ||
| C. | 0.4molHgO与0.2mol O2 | D. | 0.4molHgO |
5.下列关于物质的量的说法不正确的是( )
| A. | 物质的量的单位是mol | |
| B. | 物质的量和时间一样,也是一种物理量 | |
| C. | 通过物质的量建立起宏观数量和微观粒子数量的联系 | |
| D. | 物质的量大的物质所占体积一定就大于物质的量小的物质 |
3.能正确表示下列反应的离子方程式是( )
| A. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2(s)+2Fe3+(aq)═2Fe(OH)3(s)+3Mg2+(aq) | |
| B. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ | |
| C. | 已知:酸的强弱H2CO3>HClO>HCO3-,则:2ClO-+CO2(少量)+H2O═CO32-+2HClO | |
| D. | 将足量的NaHCO3溶液加入少量澄清石灰水中:Ca2++OH-+HCO3-═CaCO3↓+H2O |
2.下列说法正确的是( )
| A. | 催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 | |
| B. | 升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 | |
| C. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 | |
| D. | 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
20.下列关于化学用语的表示正确的是( )
0 171209 171217 171223 171227 171233 171235 171239 171245 171247 171253 171259 171263 171265 171269 171275 171277 171283 171287 171289 171293 171295 171299 171301 171303 171304 171305 171307 171308 171309 171311 171313 171317 171319 171323 171325 171329 171335 171337 171343 171347 171349 171353 171359 171365 171367 171373 171377 171379 171385 171389 171395 171403 203614
| A. | 过氧化钠的电子式:Na${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$Na | |
| B. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{80}$Br | |
| C. | 硫离子的结构示意图: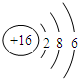 | |
| D. | 间二甲苯的结构简式: |