7.在碱性溶液中,能大量共存的离子组是( )
| A. | Mg2+?SO42-?K+?Cl- | B. | K+?Cl-?NO-3?Cu2+ | ||
| C. | Na+?SO2-4?H+?NO-3 | D. | K+?CO32-?Cl-?Na+ |
3.要证明CuSO4溶液显蓝色不是由于SO42-离子造成的,下列实验无意义的是( )
| A. | 观察K2SO4溶液的颜色 | |
| B. | 向CuSO4溶液中滴加适量的NaOH溶液,振荡后静置,溶液颜色消失 | |
| C. | 加水稀释后CuSO4溶液颜色变浅 | |
| D. | 向CuSO4溶液中滴加适量的Ba(NO3)2溶液,振荡后静置,溶液颜色未消失 |
2.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,下列反应可制取K2FeO4:2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6KCl+8H2O.对于该反应,下列说法正确的是( )
| A. | 该反应是置换反应 | |
| B. | 该反应只有K2FeO4为氧化产物 | |
| C. | 3mol氯气参与反应转移电子数为6个 | |
| D. | 该反应条件下K2FeO4的氧化性大于Cl2 |
1.将下列各种液体:①苯;②四氯化碳;③碘化钾溶液;④乙烯;⑤植物油,分别与溴水混合后充分振荡、静置,液体分为两层,原溴水层几乎是无色的是( )
| A. | ②⑤ | B. | 只有②④ | C. | ①②④⑤ | D. | ①②③④⑤ |
20.关于如图所示装置的叙述,正确的是( )
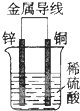

| A. | 铜片为负极 | B. | 铜片质量逐渐减少 | ||
| C. | 电子从锌片经导线流向铜片 | D. | 氢离子在铜片表面被氧化 |
19.下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp (25℃).
回答下列问题:
(1)由上表分析,若①CH3COOH ②HCO3- ③C6H5OH ④H2PO4-均可看作酸,则它们酸性由强到弱的顺序为①④③②(须填编号);
(2)写出C6H5OH与Na3PO4反应的离子方程式C6H5OH+PO43-=C6H5O-+HPO42-;
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)=c(NH4+);(填“>”、“=”或“<”)
(4)25℃时,向10mL 0.01mol/L苯酚(C6H5OH)溶液中滴加VmL 0.01mol/L氨水,混合溶液中粒子浓度关系正确的是d;
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c(NH4+)>c(C6H5O-)>c(H+)>c(OH-)
C.V=10时,混合液中水的电离程度大于10mL 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3•H2O)+2c(NH4+)=c(C6H5O-)+c(C6H5OH)
(5)如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:
①T1<T2(填>、=、<);
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法不正确的是D.
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点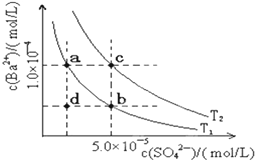
| 电解质 | 平衡方程式 | 平衡常数K | Ksp |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 | |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- | K1=4.31×10-7 K2=5.61×10-11 | |
| C6H5OH | C6H5OH?C6H5O-+H+ | 1.1×10-10 | |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- | K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 | |
| H3BO3 | 5.7×10-10 | ||
| NH3•H2O | NH3•H2O?NH4++OH- | 1.76×10-5 | |
| H2O | Kw=1.0×10-14 | ||
| Mg(OH)2 | Mg(OH)2?Mg2++2OH- | 5.6×10-12 |
(1)由上表分析,若①CH3COOH ②HCO3- ③C6H5OH ④H2PO4-均可看作酸,则它们酸性由强到弱的顺序为①④③②(须填编号);
(2)写出C6H5OH与Na3PO4反应的离子方程式C6H5OH+PO43-=C6H5O-+HPO42-;
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)=c(NH4+);(填“>”、“=”或“<”)
(4)25℃时,向10mL 0.01mol/L苯酚(C6H5OH)溶液中滴加VmL 0.01mol/L氨水,混合溶液中粒子浓度关系正确的是d;
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c(NH4+)>c(C6H5O-)>c(H+)>c(OH-)
C.V=10时,混合液中水的电离程度大于10mL 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3•H2O)+2c(NH4+)=c(C6H5O-)+c(C6H5OH)
(5)如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:
①T1<T2(填>、=、<);
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法不正确的是D.
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点

18.经测定乙烯溶解在乙醇中形成的溶液中,氧的质量分数为8%,则此溶液中氢的质量分数为( )
0 170891 170899 170905 170909 170915 170917 170921 170927 170929 170935 170941 170945 170947 170951 170957 170959 170965 170969 170971 170975 170977 170981 170983 170985 170986 170987 170989 170990 170991 170993 170995 170999 171001 171005 171007 171011 171017 171019 171025 171029 171031 171035 171041 171047 171049 171055 171059 171061 171067 171071 171077 171085 203614
| A. | 75% | B. | 13.6% | C. | 14% | D. | 25% |