10. 某学习小组围绕氯气设计了系列实验.
某学习小组围绕氯气设计了系列实验.
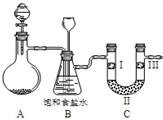
(1)用如图装置A制备氯气.选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.实验过程中,使用分液漏斗滴加液体的操作是打开分液漏斗上口活塞(或将漏斗口活塞上的凹槽与瓶口上的小孔对齐),左手顶住漏斗球,右手转动颈部活塞控制加液.
(2)装置B中饱和食盐水的作用是除去氯气中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗下端导管中液面会上升,形成水柱.
(3)为检验氯气是否具有漂白性,使氯气依次通过I、Ⅱ、Ⅲ三种物质,物质的顺序正确的是:D.
(4)为了进一步比较氧化性强弱,将一定量氯气通入溴化亚铁溶液后,再加入四氯化碳,振荡,静置,整个过程中肯定能观察到的现象是A
A.水层显棕黄色 B.水层无色 C.四氯化碳层显红棕色 D.四氯化碳层无色
(5)查阅资料后小组发现,氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,但工业上氧化卤水中I-选择了价格并不便宜的亚硝酸钠,排除环境方面的因素,可能的原因是:氯气、浓硝酸、酸性高锰酸钾等氧化性太强,还能继续氧化碘单质
(6)有人提出,工业上为防止污染空气,可用足量的NaHSO3溶液吸收余氯,试写出相应的离子反应方程式:HSO3-+Cl2+H2O═SO42-+2Cl-+3H+(或4HSO3-+Cl2═SO42-+2Cl-+3SO2↑+2H2O).判断改用NaHSO3溶液是否可行:否(填“是”或“否”).
 某学习小组围绕氯气设计了系列实验.
某学习小组围绕氯气设计了系列实验.(1)用如图装置A制备氯气.选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.实验过程中,使用分液漏斗滴加液体的操作是打开分液漏斗上口活塞(或将漏斗口活塞上的凹槽与瓶口上的小孔对齐),左手顶住漏斗球,右手转动颈部活塞控制加液.
(2)装置B中饱和食盐水的作用是除去氯气中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗下端导管中液面会上升,形成水柱.
(3)为检验氯气是否具有漂白性,使氯气依次通过I、Ⅱ、Ⅲ三种物质,物质的顺序正确的是:D.
| A | B | C | D | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
A.水层显棕黄色 B.水层无色 C.四氯化碳层显红棕色 D.四氯化碳层无色
(5)查阅资料后小组发现,氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,但工业上氧化卤水中I-选择了价格并不便宜的亚硝酸钠,排除环境方面的因素,可能的原因是:氯气、浓硝酸、酸性高锰酸钾等氧化性太强,还能继续氧化碘单质
(6)有人提出,工业上为防止污染空气,可用足量的NaHSO3溶液吸收余氯,试写出相应的离子反应方程式:HSO3-+Cl2+H2O═SO42-+2Cl-+3H+(或4HSO3-+Cl2═SO42-+2Cl-+3SO2↑+2H2O).判断改用NaHSO3溶液是否可行:否(填“是”或“否”).
9.在中和滴定中,下列操作或说法不正确的是( )
| A. | 使用滴定管时,滴定管必须用待装液润洗2~3次 | |
| B. | 酸式滴定管不能盛装碱液,碱式滴定管不能盛装酸液或强氧化性溶液 | |
| C. | 盛装准确量取的待测液的锥形瓶应预先用待测液润洗 | |
| D. | 滴定终点时,若不慎滴入过量标准溶液,可用装有待测液的滴定管再滴入一定量进行调整 |
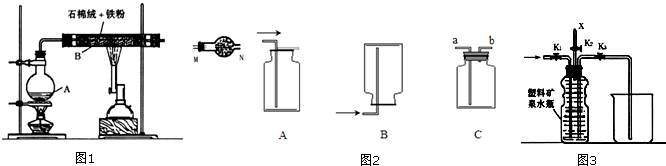
8.食盐中的加碘剂选用的是碘酸钾(KIO3)而不是碘化钾(KI).实验室可用采用如图1实验流程制备碘酸钾.
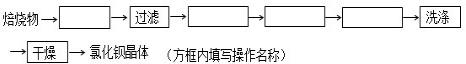
(1)操作①和操作③的名称分别为过滤、蒸馏.操作②所用到的玻璃仪器有分液漏斗.
(2)由单质碘制备碘酸钾的离子方程式为I2+5Cl2+12OH-=2IO3-+10Cl-+6H2O.
(3)问题讨论:在选择试剂X时,甲同学只选择了H2O2,乙同学除了选择H2O2外还加入了少量H2SO4,并做如下实验:
①根据乙同学选择的试剂X,写出M→N离子方程式2I-+H2O2+2H+=I2+2H2O;
②由甲、乙两同学的实验结果,你能得到的结论是:溶液的酸碱性会影响H2O2的氧化能力.
(4)实验探究:受(3)实验的启发,甲、乙同学继续探究KI固体在空气中放置变质的原因.
甲同学认为:KI变质只与空气中的O2和H2O有关;
乙同学认为:KI变质除了与O2和H2O有关外,还应与空气中的某种气体成分Y有关.
甲、乙同学分别用如图2所示装置进行实验,一段时间后取出燃烧匙中的固体,在试管中溶于淀粉溶液,结构发现甲同学试管中溶液未变蓝,而乙同学试管中溶液明显变蓝.
①气体Y为CO2(填化学式).
②KI固体在空气中变质的化学方程式为4KI+O2+2CO2=2K2CO3+I2.

(1)操作①和操作③的名称分别为过滤、蒸馏.操作②所用到的玻璃仪器有分液漏斗.
(2)由单质碘制备碘酸钾的离子方程式为I2+5Cl2+12OH-=2IO3-+10Cl-+6H2O.
(3)问题讨论:在选择试剂X时,甲同学只选择了H2O2,乙同学除了选择H2O2外还加入了少量H2SO4,并做如下实验:
| 甲 | 乙 | |
| 所选试剂X | H2O2 | H2O2,少量稀H2SO4 |
| 操作 | 向5mLM和淀粉的混合溶液中加入1mL H2O2 | 向5mLM和淀粉的混合溶液中加入1mL H2O2,再加少量稀H2SO4 |
| 实验现象 | 几秒钟后,溶液呈现很淡的蓝色 | 溶液立刻呈现较深的蓝色 |
②由甲、乙两同学的实验结果,你能得到的结论是:溶液的酸碱性会影响H2O2的氧化能力.
(4)实验探究:受(3)实验的启发,甲、乙同学继续探究KI固体在空气中放置变质的原因.
甲同学认为:KI变质只与空气中的O2和H2O有关;
乙同学认为:KI变质除了与O2和H2O有关外,还应与空气中的某种气体成分Y有关.
甲、乙同学分别用如图2所示装置进行实验,一段时间后取出燃烧匙中的固体,在试管中溶于淀粉溶液,结构发现甲同学试管中溶液未变蓝,而乙同学试管中溶液明显变蓝.
①气体Y为CO2(填化学式).
②KI固体在空气中变质的化学方程式为4KI+O2+2CO2=2K2CO3+I2.
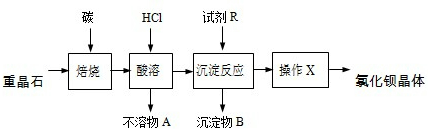
5.从废钒催化剂(主要成分V2O5、VOSO4、K2SO4、SiO2和Fe2O3等)中回收V2O5的一种生产工艺流程示意图如下:
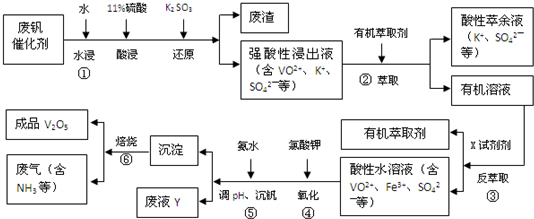
回答下列问题:
(1)①中废渣的主要成分是SiO2.
(2)②、③中的变化过程可简化为(下式中的R表示VO2+或Fe3+,HA表示有机萃取剂的主要成分):
R2(SO4)n(水层)+2n HA(有机层)?2RAn(有机层)+n H2SO4(水层).②中萃取时必须加入适量碱,其原因是加入碱中和产生的酸,平衡右移,提高钒的萃取率;③中反萃取时加入的X试剂是硫酸.
(3)完成④中反应的离子方程式:
1ClO3-+6VO2++6H+═6VO3++1(Cl-)+3(H2O)
(4)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如下表
试判断在实际生产时,⑤中加入氨水调节溶液的最佳pH为1.7;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<2.6×10-3.(已知:25℃时,Ksp(Fe(OH)3)=2.6×10-39.)
(5)写出废液Y中除H+之外的两种阳离子:Fe3+、VO3+、NH4+、K+(任写两种即可).
(6)生产时,将②中的酸性萃余液循环用于①中的水浸.在整个工艺过程中,可以循环利用的物质还有有机萃取剂、氨水(或氨气).
(7)全矾液流电池是一种新型电能储存和高效转化装置(如图所示,a、b均为惰性电极),已知:V2+为紫色,V3+为绿色,VO2+为蓝色,VO2+为黄色.当充电时,右槽溶液颜色由绿色变为紫色.则:
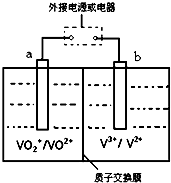
①全矾液流电池的工作原理为:VO2++V2++2H+ $?_{()电}^{()电}$VO2++H2O+V3+(请在可逆符号两侧的括号中填“充”、“放”)此时,b极接直流电源负极.
②放电过程中,a极的反应式为VO2++2H++e-=VO2++H2O,当转移1.0mol电子时共有1.0mol H+从右槽迁移进左槽(填“左”、“右”).

回答下列问题:
(1)①中废渣的主要成分是SiO2.
(2)②、③中的变化过程可简化为(下式中的R表示VO2+或Fe3+,HA表示有机萃取剂的主要成分):
R2(SO4)n(水层)+2n HA(有机层)?2RAn(有机层)+n H2SO4(水层).②中萃取时必须加入适量碱,其原因是加入碱中和产生的酸,平衡右移,提高钒的萃取率;③中反萃取时加入的X试剂是硫酸.
(3)完成④中反应的离子方程式:
1ClO3-+6VO2++6H+═6VO3++1(Cl-)+3(H2O)
(4)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如下表
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
(5)写出废液Y中除H+之外的两种阳离子:Fe3+、VO3+、NH4+、K+(任写两种即可).
(6)生产时,将②中的酸性萃余液循环用于①中的水浸.在整个工艺过程中,可以循环利用的物质还有有机萃取剂、氨水(或氨气).
(7)全矾液流电池是一种新型电能储存和高效转化装置(如图所示,a、b均为惰性电极),已知:V2+为紫色,V3+为绿色,VO2+为蓝色,VO2+为黄色.当充电时,右槽溶液颜色由绿色变为紫色.则:

①全矾液流电池的工作原理为:VO2++V2++2H+ $?_{()电}^{()电}$VO2++H2O+V3+(请在可逆符号两侧的括号中填“充”、“放”)此时,b极接直流电源负极.
②放电过程中,a极的反应式为VO2++2H++e-=VO2++H2O,当转移1.0mol电子时共有1.0mol H+从右槽迁移进左槽(填“左”、“右”).
4.工业上用洗净的废铜作原料来制备硝酸铜.为了节约原料和防止污染环境,宜采取的方法是( )
| A. | Cu$→_{△}^{H_{2}SO_{4}(浓)}$Cu(NO3)2 | B. | Cu$→_{△}^{空气}$CuO$\stackrel{HNO_{3}(稀)}{→}$Cu(NO3)2 | ||
| C. | Cu$\stackrel{HNO_{3}(稀)}{→}$Cu(NO3)2 | D. | Cu$\stackrel{HNO_{3}(浓)}{→}$Cu(NO3)2 |
3.锂被誉为“金属味精”,以LiCoO2为正极材料的锂离子电池已被广泛用作便携式电源.工业上常以β锂辉矿(主要成分为LiAlSi2O6,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂.其中一种工艺流程如下: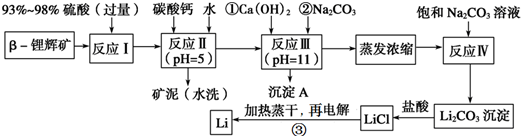
已知:部分金属氢氧化物开始沉淀和完全沉淀时的pH:
请回答下列问题:
(1)写出反应Ⅰ中有电子转移的化学方程式2FeO+4H2SO4=Fe2(SO4)3+SO2↑+H2O;
(2)反应Ⅱ加入碳酸钙的作用是除去反应Ⅰ中过量的H2SO4,控制pH,使Fe3+、Al3+完全沉淀;
(3)有同学认为在反应Ⅲ中只需加入碳酸钠溶液也能达成该步骤的目的,请阐述你的观点和理由不能,离子不能完全除去;
(4)上述流程蒸发浓缩环节,若在实验室进行该操作,当蒸发浓缩至晶体膜出现时,就可停止该操作.
(5)Li与Mg、Be与Al、B与Si这三对元素在周期表中处于对角线位置,相应的两元素及其化合物的性质有许多相似之处.这种相似性称为对角线规则.步骤③中电解时,阳极产生的氯气中会混有少量氧气,原因是加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2.
(6)请设计一种从水洗后的矿泥中分离出Al2O3的流程:矿泥$→_{过滤}^{足量NaOH}$滤液$\stackrel{足量二氧化碳}{→}$氢氧化铝$\stackrel{△}{→}$Al2O3(流程常用的表示方式为:A$→_{实验操作}^{反应试剂}$B…$→_{实验操作}^{反应试剂}$目标产物).
0 170650 170658 170664 170668 170674 170676 170680 170686 170688 170694 170700 170704 170706 170710 170716 170718 170724 170728 170730 170734 170736 170740 170742 170744 170745 170746 170748 170749 170750 170752 170754 170758 170760 170764 170766 170770 170776 170778 170784 170788 170790 170794 170800 170806 170808 170814 170818 170820 170826 170830 170836 170844 203614

已知:部分金属氢氧化物开始沉淀和完全沉淀时的pH:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
(1)写出反应Ⅰ中有电子转移的化学方程式2FeO+4H2SO4=Fe2(SO4)3+SO2↑+H2O;
(2)反应Ⅱ加入碳酸钙的作用是除去反应Ⅰ中过量的H2SO4,控制pH,使Fe3+、Al3+完全沉淀;
(3)有同学认为在反应Ⅲ中只需加入碳酸钠溶液也能达成该步骤的目的,请阐述你的观点和理由不能,离子不能完全除去;
(4)上述流程蒸发浓缩环节,若在实验室进行该操作,当蒸发浓缩至晶体膜出现时,就可停止该操作.
(5)Li与Mg、Be与Al、B与Si这三对元素在周期表中处于对角线位置,相应的两元素及其化合物的性质有许多相似之处.这种相似性称为对角线规则.步骤③中电解时,阳极产生的氯气中会混有少量氧气,原因是加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2.
(6)请设计一种从水洗后的矿泥中分离出Al2O3的流程:矿泥$→_{过滤}^{足量NaOH}$滤液$\stackrel{足量二氧化碳}{→}$氢氧化铝$\stackrel{△}{→}$Al2O3(流程常用的表示方式为:A$→_{实验操作}^{反应试剂}$B…$→_{实验操作}^{反应试剂}$目标产物).
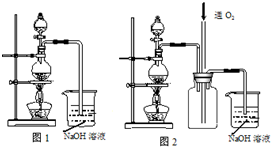 硫酸铜是一种应用极其广泛的化工原料.实验中可将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图1所示).
硫酸铜是一种应用极其广泛的化工原料.实验中可将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图1所示).