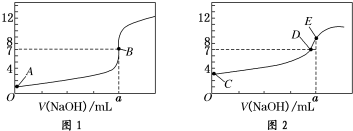
3.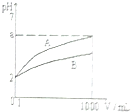 pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则列说法不正确的是( )
pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则列说法不正确的是( )
 pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则列说法不正确的是( )
pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则列说法不正确的是( )| A. | A、B两种酸溶液物质的量浓度相等 | B. | 稀释后A酸溶液的酸性比B酸溶液弱 | ||
| C. | 若A=5时,A是强酸,B是弱酸 | D. | 若5>a>2,则A、B都是弱酸 |
2.下列事实可能证明一水合氨是弱碱的是( )
| A. | 氨水能跟H2SO4反应生成(NH4)2SO4 | B. | 铵盐受热易分解 | ||
| C. | 0.1mol/L的氨水可使酚酞试液变红 | D. | 25℃,0.1mol/L氨水的pH约为12 |
1.下列方程式表示电离平衡的是( )
| A. | 4NH3(g)+5O2(g)=4NO(g)+6H2O(g) | B. | H2O+H2O=H3O++OH- | ||
| C. | NH3.H2O(aq)=NH3(g)+H2O(1) | D. | Cl2+H2O=H++Cl-+HClO |
19.电石中碳化钙可以制取乙炔气体,制取时,将反应产生的气体排水,测量出水的体积,可计算出标准状况下乙炔的体积,从而测定电石中碳化钙的含量:
(1)实验室制取乙炔气体的方程式:CaC2+2H2O→C2H2↑+Ca(OH)2
(2)若用下列仪器和导管组装实验装置:
如果所制气体流向从左向右时,上述仪器和导管从上到下,从左到右直接连接的顺序(填各仪器,导管的序号)是6接3接1接5接2接4.
(3)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次)
①称取一定量电石,置于仪器3中,塞紧橡皮塞; ②检查装置的气密性 ③在仪器6和5中注入适量水; ④待仪器3恢复至室温时,量取仪器4中水的体积(导管2中水的体积忽略不计) ⑤慢慢开启仪器6的活塞,使水逐滴滴下至不发生气体时,关闭活塞.正确操作顺序是B
A.①③②⑤④B.②①③⑤④C.①③⑤④②
(4)若实验中产生的气体存在难闻的气味,且测定结果偏大,这是因为电石中含有杂质气体,可以用硫酸铜溶液或氢氧化钠溶液加以除去.
(1)实验室制取乙炔气体的方程式:CaC2+2H2O→C2H2↑+Ca(OH)2
(2)若用下列仪器和导管组装实验装置:
| 序号 | 1 | 2 | 3 | 4 | 5 | 6 |
| 导管及仪器 |  |  | 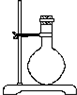 |  |  | 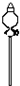 |
| 每个橡皮塞上都打了两个孔 | ||||||
(3)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次)
①称取一定量电石,置于仪器3中,塞紧橡皮塞; ②检查装置的气密性 ③在仪器6和5中注入适量水; ④待仪器3恢复至室温时,量取仪器4中水的体积(导管2中水的体积忽略不计) ⑤慢慢开启仪器6的活塞,使水逐滴滴下至不发生气体时,关闭活塞.正确操作顺序是B
A.①③②⑤④B.②①③⑤④C.①③⑤④②
(4)若实验中产生的气体存在难闻的气味,且测定结果偏大,这是因为电石中含有杂质气体,可以用硫酸铜溶液或氢氧化钠溶液加以除去.
17.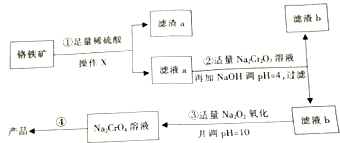 以铬铁矿(主要成分FeO•Cr2O3,含有少量SiO2等)为原料制取铬酸钠晶体(Na2CrO4)工艺流程如图所示.
以铬铁矿(主要成分FeO•Cr2O3,含有少量SiO2等)为原料制取铬酸钠晶体(Na2CrO4)工艺流程如图所示.
已知:①酸性溶液中Cr的+6价易被还原为+3价;当pH>9时Cr以CrO2-形式存在且易被氧化;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
(1)滤渣a的主要成分的化学式是SiO2;操作X用到的玻璃仪器有烧杯、玻璃棒、和漏斗.
(2)第④步得到产品涉及到的操作有蒸发浓缩、降温结晶、过滤、洗涤等.
(3)第①步反应的离子方程式是FeO+2H+=Fe2++H2O、Cr2O3+6H+=2Cr3++3H2O,第②步产生滤渣b的原因是Fe3+水解生成氢氧化铁沉淀.
(4)已知:1molAl完全燃烧放热a KJ,1mol Fe完全燃烧生成Fe3O4放热b KJ,写出Al与Fe3O4发生铝热反应的热化学方程式8Al(s)+3Fe3O4 (s)=9Fe(s)+4Al2O3 (s),△H=(8a-9b)kJ/mol.
(5)若现有224kg铬铁矿(其中含FeO•Cr2O3 50%),按上述流程最多可以得到Na2CrO4产品的质量是189kg(假设每步均恰好完全转化).
0 170601 170609 170615 170619 170625 170627 170631 170637 170639 170645 170651 170655 170657 170661 170667 170669 170675 170679 170681 170685 170687 170691 170693 170695 170696 170697 170699 170700 170701 170703 170705 170709 170711 170715 170717 170721 170727 170729 170735 170739 170741 170745 170751 170757 170759 170765 170769 170771 170777 170781 170787 170795 203614
 以铬铁矿(主要成分FeO•Cr2O3,含有少量SiO2等)为原料制取铬酸钠晶体(Na2CrO4)工艺流程如图所示.
以铬铁矿(主要成分FeO•Cr2O3,含有少量SiO2等)为原料制取铬酸钠晶体(Na2CrO4)工艺流程如图所示.已知:①酸性溶液中Cr的+6价易被还原为+3价;当pH>9时Cr以CrO2-形式存在且易被氧化;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Fe2+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.6 | |
| 沉淀完全的pH | 3.7 | 9.6 | 9(>9)溶解 |
(2)第④步得到产品涉及到的操作有蒸发浓缩、降温结晶、过滤、洗涤等.
(3)第①步反应的离子方程式是FeO+2H+=Fe2++H2O、Cr2O3+6H+=2Cr3++3H2O,第②步产生滤渣b的原因是Fe3+水解生成氢氧化铁沉淀.
(4)已知:1molAl完全燃烧放热a KJ,1mol Fe完全燃烧生成Fe3O4放热b KJ,写出Al与Fe3O4发生铝热反应的热化学方程式8Al(s)+3Fe3O4 (s)=9Fe(s)+4Al2O3 (s),△H=(8a-9b)kJ/mol.
(5)若现有224kg铬铁矿(其中含FeO•Cr2O3 50%),按上述流程最多可以得到Na2CrO4产品的质量是189kg(假设每步均恰好完全转化).
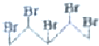
 与Br2发生加成反应,生成的产物中可能含有下列的( )
与Br2发生加成反应,生成的产物中可能含有下列的( )



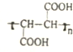 .
.