6.关于硅及其化合物的叙述中,不正确的是( )
| A. | 水玻璃可作粘合剂及耐火材料 | B. | 硅可做半导体材料 | ||
| C. | 二氧化硅是光导纤维的原料 | D. | 氮化硅陶瓷是做电子元件的材料 |
5.常温下,向一定量的稀氨水中逐滴加入物质的量浓度相同的稀盐酸,直至盐酸过量,请分析上述实验过程,并回答下列问题:
(1)该反应的离子方程式为:NH3•H2O+H+=NH4++H2O.
(2)在实验过程中,水的电离程度的变化趋势是先增大后减小.(选填“增大”、“减小”、或“不变”)
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH值,请将表中空格部分填上相应的内容,将表格补充完整:
(1)该反应的离子方程式为:NH3•H2O+H+=NH4++H2O.
(2)在实验过程中,水的电离程度的变化趋势是先增大后减小.(选填“增大”、“减小”、或“不变”)
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH值,请将表中空格部分填上相应的内容,将表格补充完整:
| 离子浓度从大到小的顺序 | 溶质化学式 | 溶液的pH值 |
| c(NH4+)>c(OH-)>c(Cl-)>c(H+) | NH4Cl、NH3.H2O | >7 |
| c(NH4+)=c(Cl-)>c(H+)=c(OH-) | NH4Cl、NH3.H2O | =7 |
c(Cl-)>c(NH4+)>c(H+)>c(OH-) | NH4Cl | <7 |
| c(Cl-)>c(H+)>c(NH4+)>c(OH-) | NH4Cl HCl | <7 |
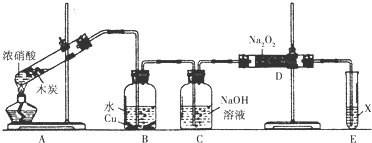
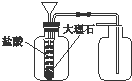
4.对于如图的叙述错误的是( )


| A. | 图示实验中发生了化学变化 | |
| B. | 液体X溶液的pH>7,液体Y是一种黑色黏稠状液体 | |
| C. | 气体Z易燃,可还原CuO,也可使溴水褪色 | |
| D. | 试管A中产生浓的白烟 |
1.下列有关实验操作或结果正确的是( )
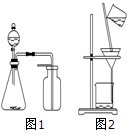

| A. | 选择合适试剂,用图1装置分别制取CO2、NO和O2 | |
| B. | 制备乙酸乙酯时,向乙醇中缓慢加入浓硫酸和冰醋酸 | |
| C. | 洗涤沉淀时(图2),向漏斗中加适量水,搅拌并滤干 | |
| D. | 用pH试纸测得0.10 mol•L-1NaF溶液的pH=5.2 |
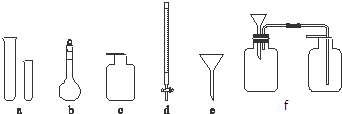
20.现要制备无水FeCl3,并将其保存下来,能选用的仪器或装置如图所示:
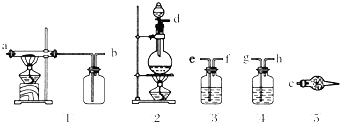
供选用的试剂如下:
A.食盐晶体 B水 C.饱和食盐水 D.烧碱溶液 E.铁粉
F.二氧化锰 G.浓硫酸 H.无水CaCl2 I.碱石灰
(1)从上述仪器中选取若干连成一个制备并保存无水FeCl3的装置,用图中各管口标号按先后可连接为d接e,f接g,h接a,b接c;
(2)填写连接装置中各选用仪器里应盛放的物质:
(3)是否需要选择装置⑤要,其原因是FeCl3易吸收空气中的水而水解,多余的Cl2可污染空气.
0 170496 170504 170510 170514 170520 170522 170526 170532 170534 170540 170546 170550 170552 170556 170562 170564 170570 170574 170576 170580 170582 170586 170588 170590 170591 170592 170594 170595 170596 170598 170600 170604 170606 170610 170612 170616 170622 170624 170630 170634 170636 170640 170646 170652 170654 170660 170664 170666 170672 170676 170682 170690 203614

供选用的试剂如下:
A.食盐晶体 B水 C.饱和食盐水 D.烧碱溶液 E.铁粉
F.二氧化锰 G.浓硫酸 H.无水CaCl2 I.碱石灰
(1)从上述仪器中选取若干连成一个制备并保存无水FeCl3的装置,用图中各管口标号按先后可连接为d接e,f接g,h接a,b接c;
(2)填写连接装置中各选用仪器里应盛放的物质:
| 仪器标号 | |||||
| 试剂标号 |
 .
. 某温度(t℃)下的溶液中,c(H+)=10-x mol/L,c(OH-)=10-y mol/L,x与y的关系如图所示.请回答下列问题:
某温度(t℃)下的溶液中,c(H+)=10-x mol/L,c(OH-)=10-y mol/L,x与y的关系如图所示.请回答下列问题: