20.下列关于物质应用的说法不正确的是( )
| A. | 用SO2漂白食品 | B. | 用硅制作太阳能电池 | ||
| C. | 工业上用氮气和氢气合成氨 | D. | 可用氢氟酸蚀刻玻璃 |
19.在密闭定容容器中,有可逆反应:nA(g)+mB(g)?pC(g)+qD(g)△H>0处于平衡状态(已知m+n>p+q),下列说法正确的是( )
①升温时C(B)/C(C)的值减小
②降温时,体系内混合气体的平均相对分子质量增大
③加入B后,A的转化率变大.
①升温时C(B)/C(C)的值减小
②降温时,体系内混合气体的平均相对分子质量增大
③加入B后,A的转化率变大.
| A. | ①②③ | B. | ②③ | C. | ①② | D. | ①③ |
17.硫氰[(SCN)2]的化学性质和卤素(X2)类似,称为拟卤素,如(SCN)2+H2O═HSCN+HSCNO,它们的阴离子的还原性强弱为Cl-<Br-<SCN-<I-.下列说法不正确的是( )
| A. | Cl2可以与KSCN溶液反应 | B. | (SCN)2可以与KI溶液反应 | ||
| C. | KSCN溶液可以与FeCl3溶液反应 | D. | (SCN)2可以与KBr溶液反应 |
16.下列关于金属钠及化合物的叙述错误的是( )
| A. | 金属钠着火时,可用泡沫灭火器来灭火 | |
| B. | Na2O2与水及CO2反应产生等量O2时,转移电子数相等 | |
| C. | 钠与熔融的四氯化钛反应可制取钛 | |
| D. | 不可用石灰水区分Na2CO3与NaHCO3溶液 |
11.下列离子方程式正确的是( )
0 170202 170210 170216 170220 170226 170228 170232 170238 170240 170246 170252 170256 170258 170262 170268 170270 170276 170280 170282 170286 170288 170292 170294 170296 170297 170298 170300 170301 170302 170304 170306 170310 170312 170316 170318 170322 170328 170330 170336 170340 170342 170346 170352 170358 170360 170366 170370 170372 170378 170382 170388 170396 203614
| A. | Cu+2H+═Cu2++H2↑ | B. | Na+H2O═Na++2OH-+H2↑ | ||
| C. | NH4++OH-═NH4OH | D. | CaCO3+2H+═Ca2++CO2↑+H2O |

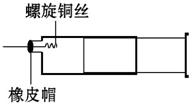 某同学采用如图装置进行实验,证明了铜与稀硝酸反应生成了NO.实验时,先向注射器内加入一定量的稀硝酸,排净注射器内的空气,迅速将带有铜丝的橡皮帽盖上,一段时间后,注射器内有无色气体产生.
某同学采用如图装置进行实验,证明了铜与稀硝酸反应生成了NO.实验时,先向注射器内加入一定量的稀硝酸,排净注射器内的空气,迅速将带有铜丝的橡皮帽盖上,一段时间后,注射器内有无色气体产生.