13.已知:2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol,下列说法不正确的是( )
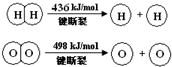

| A. | 该反应原理可用于设计氢氧燃料电池 | |
| B. | 破坏1 mol H-O键需要的能量是463.4 kJ | |
| C. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=+241.8 kJ/mol | |
| D. | H2(g)中的H-H键能比H2O(g)中的H-O键能大 |
12.下图所示的实验,不能达到实验目的是(各选项中对比溶液的浓度体积均相同)( )
| 实验方案 | 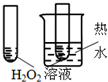 | 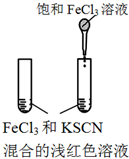 | 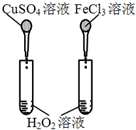 | 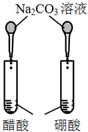 |
| 目的 | A.验证升高温度可加快H2O2分解 | B.验证增大反应物浓度对平衡的影响 | C.比较Cu2+、Fe3+对 H2O2分解速率的影响 | D.比较弱酸的 相对强弱 |
| A. | A | B. | B | C. | C | D. | D |
11.铅蓄电池的电池反应为:Pb(s)+PbO2(s)+2H2SO4(aq)$?_{充电}^{放电}$ 2PbSO4 (s)+2H2O(l).下列说法正确的是( )
| A. | 放电时,正极的反应式是:PbO2+SO42-+4H++2e-═PbSO4+2H2O | |
| B. | 放电时,电解质溶液中的H+向负极移动 | |
| C. | 充电时,阳极的电极反应为:PbSO4+2e-═Pb(s)+SO42- | |
| D. | 充电时,当有20.7gPb生成时,转移的电子为0.1mol |
10.按如图装置进行实验,若图B的X轴表示流入电极的电子的物质的量,则Y轴不可能表示的情况是( )


| A. | c (Ag+) | B. | 溶液的pH | C. | Ag棒的质量 | D. | c(NO3-) |
9.已知:2NO2 ?N2O4△H<0,CaO溶于水放热,NH4Cl晶体溶于水吸热.在3个体积相等的圆底烧瓶中充满等量的NO2气体,并分别放置在加有下列物质的烧杯(烧杯内有水)中:(1)中加入CaO,(2)中加入NH4Cl晶体,(3)中不加任何其它物质,如图所示.下列叙述正确的是( )


| A. | (1)中红综色变深,(2)中红棕色变浅 | B. | (1)中红综色变浅,(2)中红棕色变深 | ||
| C. | 烧瓶(1)中气体的压强不变 | D. | 烧瓶(2)中气体的压强增大 |
8.下列说法中,正确的是( )
| A. | 活化分子间的碰撞一定是有效碰撞 | |
| B. | 其他条件相同时,增大反应物浓度,反应物中活化分子的百分数增加 | |
| C. | 焓变和熵变都与反应的自发性有关,它们都能独立地作为自发性的判据 | |
| D. | 常温下,FeCl3溶液中由水电离出的c (H+)一定大于1×10-7mol/L |
7.一定条件下,在恒容密闭容器中,能表示反应X(g)+2Y(g)═2Z(g)一定达到化学平衡状态的是( )
| A. | 容器中的压强不再发生变化 | |
| B. | X、Y、Z的物质的量之比为1:2:2 | |
| C. | X、Y、Z的速率之比1:2:2 | |
| D. | 单位时间内生成n mol Z,同时消耗n mol Y |
6.下列电池工作时能量转化形式与其它三个不同的是( )
0 170154 170162 170168 170172 170178 170180 170184 170190 170192 170198 170204 170208 170210 170214 170220 170222 170228 170232 170234 170238 170240 170244 170246 170248 170249 170250 170252 170253 170254 170256 170258 170262 170264 170268 170270 170274 170280 170282 170288 170292 170294 170298 170304 170310 170312 170318 170322 170324 170330 170334 170340 170348 203614
| A. |  硅太阳能电池 | B. |  锌锰碱性电池 | C. |  氢燃料电池 | D. |  铅蓄电池 |
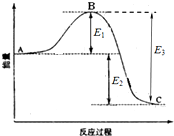 已知1mol SO2(g)生成1mol SO3(g)的能量变化如图所示.回答下列问题:
已知1mol SO2(g)生成1mol SO3(g)的能量变化如图所示.回答下列问题: