10.下列反应的离子方程式正确的是( )
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 用氯化铁溶液腐蚀电路板:Fe3++Cu═Fe2++Cu2+ |
9.实验室需用480mL 0.100mol/L的CuSO4溶液,下列配置方法正确的是( )
| A. | 称取7.68g CuSO4固体,加入 480mL水 | |
| B. | 称取12.0g 胆矾配制成 480mL溶液 | |
| C. | 称取8.0g CuSO4固体,加入 500mL水 | |
| D. | 称取12.5 g 胆矾配制成 500mL溶液 |
8.社会、生活中碰到的某些问题常常涉及到化学知识,下列说法中不正确的是( )
| A. | 全球禁用氟里昂是为了保护臭氧层不被破坏 | |
| B. | 误食重金属盐,可用喝牛奶或生鸡蛋清进行解毒 | |
| C. | 苯酚有毒,但它的稀溶液可直接用作防腐剂和消毒剂 | |
| D. | 变质的花生油有难闻的特殊气味,是由于油脂发生了水解反应 |
6.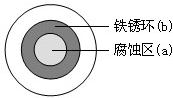 将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示.导致该现象的主要原因是液滴之下氧气含量比边缘少.下列说法正确的是( )
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示.导致该现象的主要原因是液滴之下氧气含量比边缘少.下列说法正确的是( )
 将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示.导致该现象的主要原因是液滴之下氧气含量比边缘少.下列说法正确的是( )
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示.导致该现象的主要原因是液滴之下氧气含量比边缘少.下列说法正确的是( )| A. | 液滴中的Cl-由a区向b区迁移 | |
| B. | 液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-═4OH- | |
| C. | 液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈 | |
| D. | 若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e-═Cu2+ |
5.下列离子方程式书写不正确的是( )
| A. | 少量铁粉加入稀硝酸中:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| B. | Ca(HCO3)2溶液与过量Ca(OH)2溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| C. | NH4HCO3溶液和过量Ba(OH)2溶液共热:2HCO3-+2OH-+Ba2+═BaCO3↓+CO32-+2H2O | |
| D. | Na2S溶液中通入足量H2S:S2-+H2S═2HS- |
4.用含有少量银和锌的粗铜做阳极,纯铜片做阴极,CuSO4溶液做电解液,电解一段时间后,阳极质量减少了mg,则( )
0 170026 170034 170040 170044 170050 170052 170056 170062 170064 170070 170076 170080 170082 170086 170092 170094 170100 170104 170106 170110 170112 170116 170118 170120 170121 170122 170124 170125 170126 170128 170130 170134 170136 170140 170142 170146 170152 170154 170160 170164 170166 170170 170176 170182 170184 170190 170194 170196 170202 170206 170212 170220 203614
| A. | 电解液质量增加mg | B. | 阴极质量增加xg,x>m | ||
| C. | 阴极质量增加mg | D. | 阴极质量增加yg,y<m |
 .
.