10.在强酸性溶液中一定能大量共存的离子组是( )
| A. | OH-、Na+、K+、HCO3- | B. | Na+、K+、Cl-、Ag+ | ||
| C. | Mg+、SO42-、Na+、NO3- | D. | MnO4-、Fe2+、CO32-、Ba2+ |
9.下列反应必须加入氧化剂且一步反应就能完成的是( )
| A. | N2→NH3 | B. | N2→NO | C. | N2→NO2 | D. | NO2→NO |
8.化学与社会、生活密切相关,对下列现象或解释正确的是( )
| 选项 | 应用 | 解释 |
| A | 日常生活中铝制品具有一定的抗腐蚀性 | 铝常温下不能与氧气反应 |
| B | 用氢氟酸雕刻玻璃 | 氢氟酸能与玻璃中某些成分反应 |
| C | 用酒精进行消毒 | 酒精容易挥发 |
| D | 汽车尾气中含有氮的氧化物 | 汽油中含有氮元素 |
| A. | A | B. | B | C. | C | D. | D |
7.化学与环境、材料、信息、能源关系密切,下列说法不正确的是( )
| A. | 水玻璃可用作木材的防火剂 | |
| B. | Na2O2可用于潜水员的呼吸面具中的供氧剂 | |
| C. | 对“地沟油”蒸馏可以获得汽油 | |
| D. | 石英具有很好的导光性,可用于生产光导纤维 |
6.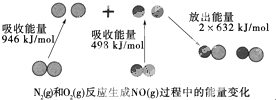 化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O(g)反应生成NO(g)过程中的能量变化:下列说法中正确的是( )
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O(g)反应生成NO(g)过程中的能量变化:下列说法中正确的是( )
 化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O(g)反应生成NO(g)过程中的能量变化:下列说法中正确的是( )
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O(g)反应生成NO(g)过程中的能量变化:下列说法中正确的是( )| A. | 1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ | |
| B. | 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 | |
| C. | 通常情况下,N2(g)和O2(g)混合能直接生成NO | |
| D. | NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
5.肼(N2H4)-空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%-30%的KOH溶液.电池总反应为:N2H4+O2═N2↑+2H2O.下列关于该燃料电池工作时的说法正确的是( )
| A. | 溶液中阴离子物质的量基本不变 | |
| B. | 正极的电极反应式是:O2+4H++4e-═2H2O | |
| C. | 正极的电极反应式是:N2H4+4OH--4e-═H2O+N2↑ | |
| D. | 溶液中阴离子向正极移动 |
4.2013年6月11日,我国“神十”载人航天飞船发射取得圆满成功.火箭发射时燃料燃烧的反应为:2N2H4(g)+2NO2(g)═3N2(g)+4H2O(l)△H=akJ/mol,关于此反应的下列说法中正确的是( )
| A. | a>0 | |
| B. | 每生成1mol水,转移8mol电子 | |
| C. | 氧化产物与还原产物的质量比为2:1 | |
| D. | N2H4是氧化剂 |
3.某种药物主要成分X的分子结构如图,关于有机物X的说法中,错误的是( )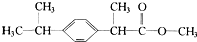

| A. | X难溶于水,易溶于有机溶剂 | B. | X能与液溴在一定条件下发生反应 | ||
| C. | X与酸、碱溶液均可以反应 | D. | X的水解产物能发生消去反应 |
2.下列混合物,不论它们以何种比例混合,只要总质量一定,经完全燃烧后产生二氧化碳和水的量也一定的是( )
| A. | 乙炔和乙苯 | B. | 甲烷和乙烷 | ||
| C. | 乙醛和丙酮 | D. | 乙酸和乳酸[CH3CH(OH)COOH] |
1.短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同.X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,Y的性质稳定,而Z不能形成双原于分子.根据以上叙述,下列说法中正确的是( )
0 170001 170009 170015 170019 170025 170027 170031 170037 170039 170045 170051 170055 170057 170061 170067 170069 170075 170079 170081 170085 170087 170091 170093 170095 170096 170097 170099 170100 170101 170103 170105 170109 170111 170115 170117 170121 170127 170129 170135 170139 170141 170145 170151 170157 170159 170165 170169 170171 170177 170181 170187 170195 203614
| A. | W与Y可形成既含极性共价键又含非极性共价键的化合物 | |
| B. | W、X、Y、Z原子的核外最外层电子数的总和为20 | |
| C. | 上述四种元素的原子半径大小为W<X<Y<Z | |
| D. | 由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |