题目内容
3.某种药物主要成分X的分子结构如图,关于有机物X的说法中,错误的是( )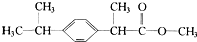
| A. | X难溶于水,易溶于有机溶剂 | B. | X能与液溴在一定条件下发生反应 | ||
| C. | X与酸、碱溶液均可以反应 | D. | X的水解产物能发生消去反应 |
分析 该物质中含有苯环、酯基,具有苯和酯的性质,能发生加成反应、氧化反应、取代反应、水解反应,据此分析解答.
解答 解:A.该物质中不含亲水基,所以难溶于水,易溶于有机溶剂,故A正确;
B.含有苯环,在一定条件下能和液溴发生取代反应,故B正确;
C.含有酯基,在酸性或碱性条件下都能发生水解反应,故C正确;
D.X是水解产物是甲醇与芳香酸,甲醇只含一个C原子,不能发生消去反应,故D错误;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,注意醇发生消去反应时醇结构特点,为易错点.

练习册系列答案
相关题目
14.板蓝根速效感冒冲剂的主要成分之一为“对乙酰氨基酚”,其结构简式为: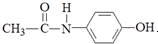 ,有关它的性质描述错误的是( )
,有关它的性质描述错误的是( )
 ,有关它的性质描述错误的是( )
,有关它的性质描述错误的是( )| A. | 它能与NaOH溶液反应 | |
| B. | 其水解产物之一对氨基苯酚(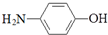 )具有弱酸性、弱碱性和强还原性 )具有弱酸性、弱碱性和强还原性 | |
| C. | 与对硝基乙苯互为同分异构体 | |
| D. | 1mol该物质与浓溴水反应时最多消耗Br23mol |
11.下列实验不能达到预期目的是( )
①淀粉加稀硫酸水解后,立即加入新制氢氧化铜溶液,可以检验产物是否含有葡萄糖
②可以用NaOH溶液除去溴苯中混有的少量溴
③向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,则该溶液中一定有SO42-
④用加热的方法提取NH4Cl固体中混有的少量碘
⑤用溴的四氯化碳溶液验证汽油中是否含有不饱和烃.
①淀粉加稀硫酸水解后,立即加入新制氢氧化铜溶液,可以检验产物是否含有葡萄糖
②可以用NaOH溶液除去溴苯中混有的少量溴
③向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,则该溶液中一定有SO42-
④用加热的方法提取NH4Cl固体中混有的少量碘
⑤用溴的四氯化碳溶液验证汽油中是否含有不饱和烃.
| A. | ①④⑤ | B. | ②③⑤ | C. | ②④⑤ | D. | ①③④ |
18.下列有关化学键与晶体结构的叙述正确的是( )
| A. | 离子晶体在熔化时,离子键被破坏;而分子晶体熔化时,化学键不被破坏 | |
| B. | 12g金刚石中,含C-C共价键键数为4mol | |
| C. | 水晶、干冰熔化时克服粒子间作用力的类型相同 | |
| D. | 熔点由高到低的顺序是:晶体硅>碳化硅>金刚石 |
8.化学与社会、生活密切相关,对下列现象或解释正确的是( )
| 选项 | 应用 | 解释 |
| A | 日常生活中铝制品具有一定的抗腐蚀性 | 铝常温下不能与氧气反应 |
| B | 用氢氟酸雕刻玻璃 | 氢氟酸能与玻璃中某些成分反应 |
| C | 用酒精进行消毒 | 酒精容易挥发 |
| D | 汽车尾气中含有氮的氧化物 | 汽油中含有氮元素 |
| A. | A | B. | B | C. | C | D. | D |
15.常温下0.1mol/LNH3•H2O的pH=a,下列能使溶液pH=a-1的措施是( )
| A. | 加水,使溶液体积变为原来的10倍 | B. | 升高温度(不考虑NH3的挥发) | ||
| C. | 加入适量的NH4Cl固体 | D. | 加入等体积0.2mol/L的氢氧化钠 |
13.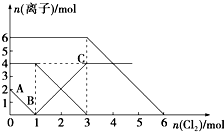 已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )
已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )
 已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )
已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )| A. | 还原性:I->Fe2+>Br- | |
| B. | 原混合溶液中FeBr2的物质的量为6 mol | |
| C. | 当通入2 mol Cl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| D. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
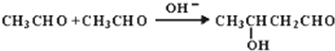

 .E中含氧官能团的名称为羟基、醛基.
.E中含氧官能团的名称为羟基、醛基.