8.能源可划分为一级能源和二级能源.自然界中以形成形式提供的能源称为一级能源,需依靠其他能源间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取:2H2O(l)═2H2(g)+O2(g)下列叙述正确的是( )
| A. | 电源是一级能源 | B. | 天然气是一级能源 | ||
| C. | 水力是二级能源 | D. | 干馏煤气是一级能源 |
7.核电荷数为16的元素和核电荷数为4的原子相比较,前者的下列数据是后者的4倍的是( )
| A. | 原子半径 | B. | 最外层电子数 | C. | 电子层数 | D. | 次外层电子数 |
6.汽车尾气中NO,是造成大气污染的物质之一,但NO又是工业生产硝酸的中间产物,另外NO在人体中的血管内又有传送信息的功能,下列有关NO的说法正确的是( )
| A. | NO是一种红棕色气体,易溶于水 | |
| B. | 汽车尾气中NO的来源是空气中的N2与O2在汽车气缸内的高温环境下的反应产物 | |
| C. | 工业生产硝酸的原料主要有NO和空气 | |
| D. | 由于NO在血管中的特殊作用,所以NO无毒 |
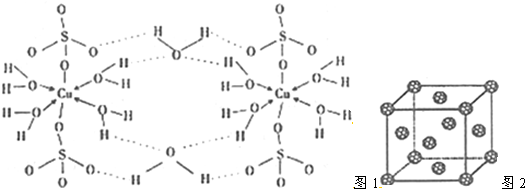
5.(1)胆矾CuSO4•5H2O的结构示意图1如下,其含有的微粒间作用力有abde(填序号)
a.离子键 b.极性键 c.金属键 d.配位键 e.氢键 f.非极性键
(2)根据等电子原理,写出与CO2等电子体的分子和离子各一种N2O或CS2、CNO-或SCN-或NO2+;1molO22+中含有的π键数目为2NA
(3)已知
分析表中四种物质的相关数据,请回答
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4;但氨气分子间还存在氢键,则NH3的沸点高于PH3
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是C-H键的键能大于Si-H键的键能,N-H键的键能大于P-H键的键能,因此分解温度CH4的分解温度高于SiH4,NH3的分解温度高于PH3
(4)C60形成晶体的晶胞结构如图2所示,则每个C60分子周围距离最近的C60分子由12个,若晶胞参数为pnm,列出计算该晶体的密度$\frac{4×720}{(p×1{0}^{-7})^{3}{N}_{A}}$g•cm-3(阿伏伽德罗常数用NA表示)
a.离子键 b.极性键 c.金属键 d.配位键 e.氢键 f.非极性键
(2)根据等电子原理,写出与CO2等电子体的分子和离子各一种N2O或CS2、CNO-或SCN-或NO2+;1molO22+中含有的π键数目为2NA
(3)已知
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4;但氨气分子间还存在氢键,则NH3的沸点高于PH3
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是C-H键的键能大于Si-H键的键能,N-H键的键能大于P-H键的键能,因此分解温度CH4的分解温度高于SiH4,NH3的分解温度高于PH3
(4)C60形成晶体的晶胞结构如图2所示,则每个C60分子周围距离最近的C60分子由12个,若晶胞参数为pnm,列出计算该晶体的密度$\frac{4×720}{(p×1{0}^{-7})^{3}{N}_{A}}$g•cm-3(阿伏伽德罗常数用NA表示)

3.下列说法正确的是( )
| A. | 能自发进行的化学反应,一定是△H<0,△S>0 | |
| B. | 常温下5.0×10-3mol•L-1KHA溶液的pH=3.75,该溶液中c(A2-)<c(H2A) | |
| C. | 室温时,M(0H)2(s)?M2+(aq)+2OH-(aq) Ksp=a;c(M2+)=bmol•L-1时,溶液的pH等于14+$\frac{1}{2}$lg($\frac{b}{a}$) | |
| D. | Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4) |
2.分子式为C6H12O2并能与饱和碳酸氢钠溶液反应放出气体的有机物有(不含立体异构)( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 8种 |
1.用A+、B+、C-、D-四种一价离子组成四种盐AC、BD、AD、BC.在室温下其1mol•L-1的溶液,前两种溶液的pH=7,第三种溶液的pH>7,最后一种溶液pH<7,则有关判断正确的是( )
| A | B | C | D | |
| 碱性 | AOH>BOH | AOH<BOH | AOH>BOH | AOH<BOH |
| 酸性 | HC>HD | HC>HD | HC<HD | HC<HD |
| A. | A | B. | B | C. | C | D. | D |
20.室温下,下列有关两种溶液的说法不正确的是( )
| 序号 | ① | ② |
| pH | 12 | 12 |
| 溶液 | 氨水 | 氢氧化钠溶液 |
| A. | ①②两溶液中c(OH-)相等 | |
| B. | ①②两溶液分别加水稀释10倍,稀释后溶液的pH:①>② | |
| C. | ①溶液的物质的量浓度为0.01mol•L-1 | |
| D. | 等体积的①②两溶液分别与0.01 mol•L-1的盐酸完全中和,消耗盐酸的体积:①>② |
19.可逆反应在一定条件下达到化学平衡状态的标志是( )
0 169800 169808 169814 169818 169824 169826 169830 169836 169838 169844 169850 169854 169856 169860 169866 169868 169874 169878 169880 169884 169886 169890 169892 169894 169895 169896 169898 169899 169900 169902 169904 169908 169910 169914 169916 169920 169926 169928 169934 169938 169940 169944 169950 169956 169958 169964 169968 169970 169976 169980 169986 169994 203614
| A. | 反应停止了 | B. | 正反应速率与逆反应速率相等 | ||
| C. | 反应物和生成物浓度相等 | D. | 正反应速率与逆反应速率均为零 |
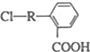 (其中R为饱和烃基),X在一定条件下如图所示的转化关系,已知Q的蒸气密度是相同条件下H2密度的74倍,分子组成符号CaHbO2
(其中R为饱和烃基),X在一定条件下如图所示的转化关系,已知Q的蒸气密度是相同条件下H2密度的74倍,分子组成符号CaHbO2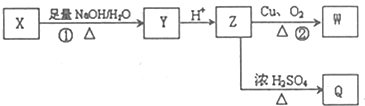
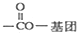 ),写出任意一种能发生银镜反应的符合上述条件的物质的结构简式
),写出任意一种能发生银镜反应的符合上述条件的物质的结构简式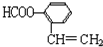
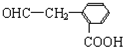 .于由X通过一步反应得到P,该反应的化学方程式是
.于由X通过一步反应得到P,该反应的化学方程式是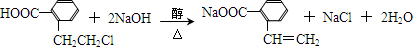
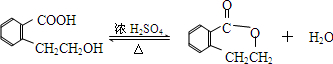 .
.