18. 我国首创的海洋电池以铝板、铂网作电极,海水为电解质溶液,电池总反应为:4Al+3O2+6H2O═4Al(OH)3.下列关于该电池的说法不正确的是( )
我国首创的海洋电池以铝板、铂网作电极,海水为电解质溶液,电池总反应为:4Al+3O2+6H2O═4Al(OH)3.下列关于该电池的说法不正确的是( )
 我国首创的海洋电池以铝板、铂网作电极,海水为电解质溶液,电池总反应为:4Al+3O2+6H2O═4Al(OH)3.下列关于该电池的说法不正确的是( )
我国首创的海洋电池以铝板、铂网作电极,海水为电解质溶液,电池总反应为:4Al+3O2+6H2O═4Al(OH)3.下列关于该电池的说法不正确的是( )| A. | 铝板是电池的正极 | |
| B. | 电池工作时铝板逐渐被消耗 | |
| C. | 电池工作时实现了化学能向电能的转化 | |
| D. | 将铂电极做成网状,可增大与氧气的接触面积 |
17.下列过程吸收热量的是( )
| A. | 硝酸铵和适量的水混合 | B. | 氧化钙和适量的水混合 | ||
| C. | 稀盐酸与金属镁反应 | D. | 汽油在空气中燃烧 |
16.下列元素或物质性质的比较中,正确的是( )
| A. | 元素的最高正化合价:N>S | B. | 热稳定性:HCl>HI | ||
| C. | 碱性:Mg(OH)2>NaOH | D. | 酸性:H2SiO3>H2CO3 |
15.下列实验装置或操作能达到实验目的是( )
| A. | 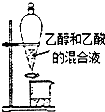 分离乙醇和乙酸 | B. | 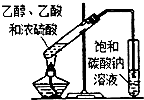 制取乙酸乙酯 制取乙酸乙酯 | C. | 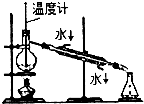 石油的蒸馏 石油的蒸馏 | D. | 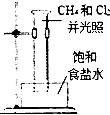 甲烷与氯气反应 |
14.下列物质互为同分异构体的一组是( )
| A. | 乙烷和乙烯 | B. | 金刚石和石墨 | ||
| C. | 乙醇和二甲醚 | D. | 一氧化碳和二氧化碳 |
13.下列物质属于共价化合物的是( )
| A. | CaBr2 | B. | NaHCO3 | C. | H2 | D. | C6H6 |
12.某锂电池的电池总反应为4Li+2SOCl2═4LiCl+S+SO2,下列有关说法错误的是( )
| A. | 锂电极作电池负极,放电过程中发生氧化反应 | |
| B. | 1molSOCl2发生电极反应转移的电子数为2mol | |
| C. | 电池的正极反应为2SOCl2+2e-═4Cl-+S+SO2 | |
| D. | 组装该电池必须在无水、无氧的条件下进行 |
11.在一定温度下,向a L密闭容器中加入一定量A、B气体,发生如下反应:A2(g)+3B(g)?2C2 (g)+2D(g),下列叙述能说明该反应达到化学平衡状态的是( )
| A. | 容器中总压强不再随时间而变化 | |
| B. | v正(B)=0.03mol/(L•s),v逆(D)=1.2mol/(L•min) | |
| C. | 单位时间内断裂一个A-A键,同时生成两个C-C键 | |
| D. | 容器中混合气体的密度不再随时间而变化 |
10.下列分子式所表示的物质的同分异构体数目最多的是(不考虑立体异构)( )
| A. | CH2Cl2 | B. | C2H2Cl2 | C. | C4H8 | D. | C3H7Cl |
9.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
0 169247 169255 169261 169265 169271 169273 169277 169283 169285 169291 169297 169301 169303 169307 169313 169315 169321 169325 169327 169331 169333 169337 169339 169341 169342 169343 169345 169346 169347 169349 169351 169355 169357 169361 169363 169367 169373 169375 169381 169385 169387 169391 169397 169403 169405 169411 169415 169417 169423 169427 169433 169441 203614
| A. | 标准状况下,5.6L四氯化碳含有的分子数为0.25NA | |
| B. | 16g O2和 O3的混合气体中,含有的氧原子数是1.5NA | |
| C. | 1 mol苯分子中含有的碳碳双键数为3NA | |
| D. | 1 mol${\;}_{8}^{16}$OD- 中含有的质子数、中子数均为9NA |