1.有A、B、C、D、E五种短周期原子序数依次增大,其相关信息如表.
(1)C的基态原子核外电子排布式1s22s22p4;
(2)B2分子中σ 键与π键个数之比是1:2;
(3)已知常温下1g A单质在C单质中燃烧生成稳定的液态物质时放出142.9kJ热量,则表示单质A燃烧热的化学方程式为H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol;
(4)A、B、C三种元素组成一个强酸弱碱盐的化学式为NH4NO3,该物质的晶体类型是离子晶体,其水溶液中各种离子浓度由大到小顺序为c(NO3-)>c(NH4+)>c(H+)>c(OH-).
| 元素 | 相关信息 |
| A | 原子半径是周期表所有元素中最小的 |
| B | 单质常温下为双原子分子,其氢化物水溶液使酚酞变红 |
| C | 基态原子核外S能级上有电子,且p能级上只有一个轨道排满 |
| D | 同周期中电负性最小 |
| E | E的族序数与周期数之差为4 |
(2)B2分子中σ 键与π键个数之比是1:2;
(3)已知常温下1g A单质在C单质中燃烧生成稳定的液态物质时放出142.9kJ热量,则表示单质A燃烧热的化学方程式为H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol;
(4)A、B、C三种元素组成一个强酸弱碱盐的化学式为NH4NO3,该物质的晶体类型是离子晶体,其水溶液中各种离子浓度由大到小顺序为c(NO3-)>c(NH4+)>c(H+)>c(OH-).
20.下列关于元素周期表的结构的叙述中正确的是( )
0 168610 168618 168624 168628 168634 168636 168640 168646 168648 168654 168660 168664 168666 168670 168676 168678 168684 168688 168690 168694 168696 168700 168702 168704 168705 168706 168708 168709 168710 168712 168714 168718 168720 168724 168726 168730 168736 168738 168744 168748 168750 168754 168760 168766 168768 168774 168778 168780 168786 168790 168796 168804 203614
| A. | 除短周期外,其他周期均有18种元素 | |
| B. | 副族元素中没有非金属元素 | |
| C. | 周期表中的第三列是ⅢA | |
| D. | 在过渡元素区能找到大量单质半导体材料 |

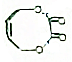 ,写出其合成路程图.
,写出其合成路程图.
 .
. (任写一种).
(任写一种). 为原料制备
为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:


 (R、R′表示烃基或氢)
(R、R′表示烃基或氢) ,E的结构简式是CH3CHO.
,E的结构简式是CH3CHO.
 .
.