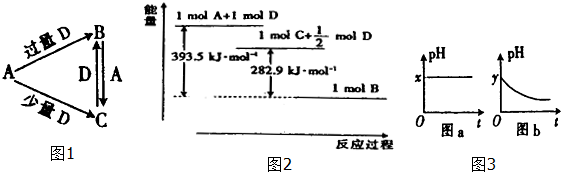
20.下列反应中,反应后固体物质增重的是( )
| A. | 氢气通过灼热的氧化铜粉末 | B. | 二氧化碳通过过氧化钠粉末 | ||
| C. | 铝与氧化铁发生铝热反应 | D. | 将锌粒投入硝酸铜溶液中 |
19.下列实验过程中,始终无明显现象的是( )
| A. | Cl2通入Na2CO3溶液中 | B. | CO2通入CaCl2溶液中 | ||
| C. | NH3通入AgNO3溶液中 | D. | SO2通入NaHS溶液中 |
18.微粒有多种表示方式,下列各组不同表示方式一定代表同种微粒的是( )
| A. | C3H6、CH2═CHCH3 | B. | H2O2、 | C. | 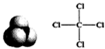 | D. |  1S22S22p63S23p6 1S22S22p63S23p6 |
17.最近媒体报道了一些化学物质,如:爆炸力极强的N5、比黄金还贵的18O、太空中的甲醇气团等.下列说法中正确的是( )
| A. | 18O2和16O2是两种不同的原子 | B. | 甲醇(CH3OH)属于离子化合物 | ||
| C. | N5和N2是氮元素的两种同位素 | D. | 由N5变成N2是化学变化 |
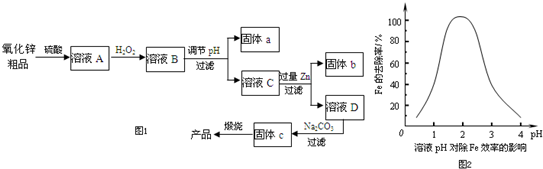
15.C、O、Si、Cl、Na、Fe是中学化学中常见的六种元素.
(1)Si位于元素周期表第三周期第ⅣA族,Fe2+的离子结构示意图为 ,Cl的基态原子外围电子层排布式为3s23p5;
,Cl的基态原子外围电子层排布式为3s23p5;
(2)用“>”或“<”填空:
(3)氯的一种常见含氧酸有漂白性,它与H2CO3酸性强弱不同,写出可以证明此结论一个化学方程式Ca(ClO)2+CO2+H2O═CaCO3+2HClO;
(4)黄绿色气体二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂.工业上常利用氯酸钠和浓盐酸来制备ClO2,同时还得到一种黄绿色的气体单质、一种无色液体和一种常见离子化合物.写出该反应的化学方程式,并标出电子转移的方向和数目: ;
;
(5)Ti倍称为继铁铝之后“21世纪”金属,应用前景很广.钛铁矿(FeTiO3)可被一氯化碳还原为铁和TiO2固体.在25℃、101KPa下,已知煤消耗7克CO,吸收aKJ热量,该反应的热化学方程式为FeTiO3(s)+CO(g)=TiO2(s)+Fe(s)+CO2(g))△H=+4aKJ•mol-1.
(1)Si位于元素周期表第三周期第ⅣA族,Fe2+的离子结构示意图为
 ,Cl的基态原子外围电子层排布式为3s23p5;
,Cl的基态原子外围电子层排布式为3s23p5;(2)用“>”或“<”填空:
| 第一电离能 | 键能 | 沸点 |
| O>Na | H-Cl>H-Si | CO2<H2O |
(4)黄绿色气体二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂.工业上常利用氯酸钠和浓盐酸来制备ClO2,同时还得到一种黄绿色的气体单质、一种无色液体和一种常见离子化合物.写出该反应的化学方程式,并标出电子转移的方向和数目:
 ;
;(5)Ti倍称为继铁铝之后“21世纪”金属,应用前景很广.钛铁矿(FeTiO3)可被一氯化碳还原为铁和TiO2固体.在25℃、101KPa下,已知煤消耗7克CO,吸收aKJ热量,该反应的热化学方程式为FeTiO3(s)+CO(g)=TiO2(s)+Fe(s)+CO2(g))△H=+4aKJ•mol-1.
14.室温下,下列溶液中粒子浓度大小关系正确的是( )
0 168508 168516 168522 168526 168532 168534 168538 168544 168546 168552 168558 168562 168564 168568 168574 168576 168582 168586 168588 168592 168594 168598 168600 168602 168603 168604 168606 168607 168608 168610 168612 168616 168618 168622 168624 168628 168634 168636 168642 168646 168648 168652 168658 168664 168666 168672 168676 168678 168684 168688 168694 168702 203614
| A. | Na2S溶液中,2c(Na+)=c(S2-)+c(HS-)+c(H2S) | |
| B. | 强碱弱酸盐NaA溶液的pH=8,则c(OH-)-c(HA)=1,0×10-8mol/L | |
| C. | KAl(SO4)2溶液中,c(SO42-)>c(K+)=c(Al3+)>c(H+)>c(OH-) | |
| D. | 向100ml pH=12 的 NaOH溶液中加入pH=2的醋酸溶液至中性,所得溶液的总体积大于200ml |
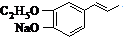 .
.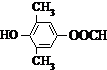 或
或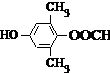 .
.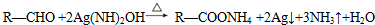 .
.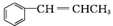 为原料制备
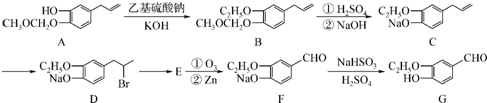
为原料制备 的合成路线流程图如下,试在方框内补充有机物的结构简式:
的合成路线流程图如下,试在方框内补充有机物的结构简式: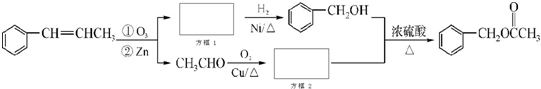
 ,D的核磁共振氢谱图中将出现4种峰;
,D的核磁共振氢谱图中将出现4种峰; ;
;