17.下列说法正确的是( )
| A. | 原子最外层电子数为2的元素一定处于周期表ⅡA族 | |
| B. | 同周期第IA族元素与第ⅦA族元素形成的是离子化合物 | |
| C. | 硫化氢的沸点比水的沸点高 | |
| D. | 同主族元素形成的氧化物的晶体类型均相同 |
16.下列排列顺序正确的是( )
| A. | 粒子半径:Al3+>Mg2+>F- | B. | 热稳定性:HI>HBr>HCl>HF | ||
| C. | 酸性:H2SiO3<H3PO4<H2SO4<HClO4 | D. | 碱性:Al(OH)3>Mg(OH)2>NaOH |
15.下列反应属于吸热反应的是( )
| A. | 燃烧木炭 | B. | 酸碱中和反应 | ||
| C. | 锌粒与稀硫酸反应制取H2 | D. | Ba(OH)2•8H2O与NH4Cl反应 |
14.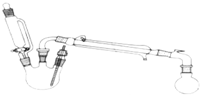 某研究性小组探究乙酸乙酯的反应机理,实验如下:已知:相关物理性质(常温常压)
某研究性小组探究乙酸乙酯的反应机理,实验如下:已知:相关物理性质(常温常压)
合成反应:在三颈烧瓶中加入乙醇5mL,硫酸5mL,2小片碎瓷片.漏斗加入乙酸14.3mL,乙醇20mL.冷凝管中通入冷却水后,开始缓慢加热,控制滴加速度等于蒸馏速度,反应温度不超过120℃.分离提纯:将反应粗产物倒入分液漏斗中,依次用少量饱和的Na2CO3溶液、饱和NaCl溶液、饱和CaCl2溶液洗涤,分离后加入无水碳酸钾,静置一段时间后弃去碳酸钾.最终通过蒸馏得到纯净的乙酸乙酯. 回答下列问题:
(1)制取乙酸乙酯化学方程式为:CH3COOH+CH3CH2OH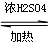 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.
(2)浓硫酸与乙醇如何混合?先向三颈烧瓶加入乙醇,再沿着瓶壁缓慢加入浓硫酸,边振荡边滴加.
(3)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)控制滴加乙酸和乙醇混和液的速度等于蒸馏速度目的是?保证乙醇量是乙酸量10倍以上,提高乙酸的转化率.
(5)蒸出的粗乙酸乙酯中主要有哪些杂质?乙醚、乙酸、乙醇和水.
(6)饱和的Na2CO3溶液洗涤除去乙酸,能否换成NaOH溶液?若不能,为什么?(用化学方程式表示)不能;CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH.用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,为什么不用水?减少乙酸乙酯溶解.
 某研究性小组探究乙酸乙酯的反应机理,实验如下:已知:相关物理性质(常温常压)
某研究性小组探究乙酸乙酯的反应机理,实验如下:已知:相关物理性质(常温常压)| 密度g/mL | 熔点/℃ | 沸点/℃ | 水溶性 | |
| 乙醇 | 0.79 | -114 | 78 | 溶 |
| 乙酸 | 1.049 | 16.2 | 117 | 溶 |
| 乙酸乙酯 | 0.902 | -84 | 76.5 | 不溶 |
(1)制取乙酸乙酯化学方程式为:CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.(2)浓硫酸与乙醇如何混合?先向三颈烧瓶加入乙醇,再沿着瓶壁缓慢加入浓硫酸,边振荡边滴加.
(3)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)控制滴加乙酸和乙醇混和液的速度等于蒸馏速度目的是?保证乙醇量是乙酸量10倍以上,提高乙酸的转化率.
(5)蒸出的粗乙酸乙酯中主要有哪些杂质?乙醚、乙酸、乙醇和水.
(6)饱和的Na2CO3溶液洗涤除去乙酸,能否换成NaOH溶液?若不能,为什么?(用化学方程式表示)不能;CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH.用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,为什么不用水?减少乙酸乙酯溶解.
12.(1)①下表为烯烃类化合物与溴发生加成反应的相对速率(以乙烯为标准).
据表中数据,总结烯烃类化合物加溴时,反应速率与C=C上取代基的种类、个数间的关系:C=C上取代基为烃基的反应速率快,烃基越多反应速率越快,C=C上取代基为卤素原子的反应速率慢,卤素原子越多反应速率越慢.
②下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是D.
A.(CH3)2C=C(CH3) 2 B.CH3CH=CHCH3C.CH2CH=CH2 D.CH2=CHCl
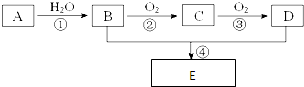
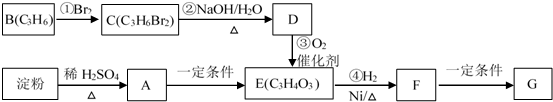
(2)已知A是化工生产中重要的气态烃,在标准状况下的密度为1.25g/L,现以A为主要原料合成E,其合成路线如图所示.回答下列问题:①写出A的电子式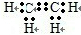 .
.
②写出下列反应的化学方程式:
第①步CH2=CH2+H2O→CH3CH2OH;
第③步2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH;
③已知A在有催化剂条件下可以与氧气反应直接制得C,写出该反应的化学方程式2CH2=CH2+O2$\stackrel{催化剂}{→}$2CH3CHO
| 烯烃类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
②下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是D.
A.(CH3)2C=C(CH3) 2 B.CH3CH=CHCH3C.CH2CH=CH2 D.CH2=CHCl
(2)已知A是化工生产中重要的气态烃,在标准状况下的密度为1.25g/L,现以A为主要原料合成E,其合成路线如图所示.回答下列问题:①写出A的电子式
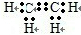 .
.②写出下列反应的化学方程式:
第①步CH2=CH2+H2O→CH3CH2OH;
第③步2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH;
③已知A在有催化剂条件下可以与氧气反应直接制得C,写出该反应的化学方程式2CH2=CH2+O2$\stackrel{催化剂}{→}$2CH3CHO

10.有机物CH2=CH-CH2-CH(OH)-COOH可发生下列反应中的哪几类( )
(1)使溴水褪色 (2)使高锰酸钾溶液褪色 (3)与钠反应 (4)加聚反应
(5)酯化反应 (6)水解反应 (7)取代反应.
(1)使溴水褪色 (2)使高锰酸钾溶液褪色 (3)与钠反应 (4)加聚反应
(5)酯化反应 (6)水解反应 (7)取代反应.
| A. | 除(7)外都可以 | B. | 除(6)外都可以 | C. | (1)(2)(3)(7) | D. | (1)(2)(3)(5) |
9.苯分子中六个碳-碳键是完全等同的,不是单双键交替结构,下列事实可以作为证据的是( )
①苯不能使溴的CCl4溶液褪色;②苯不能使酸性高锰酸钾溶液褪色;③苯在一定条件下既能发生取代反应,又能发生加成反应;④经测定,邻二甲苯只有一种结构;⑤苯的一氯代物只有一种.
①苯不能使溴的CCl4溶液褪色;②苯不能使酸性高锰酸钾溶液褪色;③苯在一定条件下既能发生取代反应,又能发生加成反应;④经测定,邻二甲苯只有一种结构;⑤苯的一氯代物只有一种.
| A. | ①②④⑤ | B. | ①②③⑤ | C. | ①②④ | D. | ①②③④ |
8.下列有机物命名正确的是( )
0 167718 167726 167732 167736 167742 167744 167748 167754 167756 167762 167768 167772 167774 167778 167784 167786 167792 167796 167798 167802 167804 167808 167810 167812 167813 167814 167816 167817 167818 167820 167822 167826 167828 167832 167834 167838 167844 167846 167852 167856 167858 167862 167868 167874 167876 167882 167886 167888 167894 167898 167904 167912 203614
| A. | 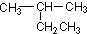 2-乙基丙烷 2-乙基丙烷 | B. | 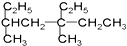 3,5-二甲基-3-乙基庚烷 3,5-二甲基-3-乙基庚烷 | ||
| C. | 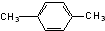 间二甲苯 间二甲苯 | D. | 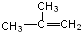 2-甲基-2-丙烯 2-甲基-2-丙烯 |
 .
.