7.下列叙述错误的是( )
| A. | 活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同 | |
| B. | FeO在空气中受热会迅速转变为Fe2O3 | |
| C. | Na2SiO3溶液俗称水玻璃,可用于制备硅胶和木材防火剂 | |
| D. | 制作“毒豆芽”所用的亚硝酸钠、“小苏打水”中的碳酸氢钠都属于钠盐 |
6.NA代表阿伏伽德罗常数的值,已知C2H4和C3H6的混合物的质量为ag,则该混合物( )
| A. | 所含共用电子对数为($\frac{a}{7}+1$)NA | B. | 所含碳氢键数目为$\frac{a{N}_{A}}{7}$ | ||
| C. | 燃烧时消耗的O2一定是$\frac{33.6a}{14}$L | D. | 所含原子总数为$\frac{a{N}_{A}}{14}$ |
5.分子式为C7H2402的有机物Q,在稀硫酸存在下能发生反应生成M、N,其中M的相对分子质量为60,下列有关说法中一定正确的是( )
| A. | Q可能有8种同分异构体 | B. | Q不可能有4种同分异构体 | ||
| C. | N只有2种同分异构体 | D. | M只有4种同分异构体 |
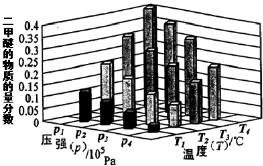
3.根据下列有关图象判断,下列说法正确的是( )


| A. | 由图象Ⅰ可知,该反应在T1、T3处达到平衡 | |
| B. | 由图象Ⅰ可知,该反应的△H>0 | |
| C. | 图象Ⅱ发生反应的化学方程式为2X+6Y?3Z | |
| D. | 由图象Ⅱ可知,相同条件下起始时投入0.1mol•L-1 Y、0.3mol•L-1 Z和0.4mol•L-1 Z反应,达到平衡后,Z的浓度为0.4mol•L-1 |
2.短周期元素离子aA2+、bB+、cC3+、dD- 都具有相同电子层结构,则下列叙述正确的是( )
| A. | 原子半径B>A>D | B. | 离子半径C>D>B>A | ||
| C. | 单质还原性A>B>D>C | D. | A、B、C、D可能是第二周期元素 |
20.某饱和一元酸跟足量金属钠反应生成0.5gH2.等量的该醇经充分燃烧后生成H2O36g.则该醇应是( )
| A. | 甲醇 | B. | 乙醇 | C. | 丙醇 | D. | 丁醇 |
18.关于元素周期表,下列叙述中不正确的是( )
0 167661 167669 167675 167679 167685 167687 167691 167697 167699 167705 167711 167715 167717 167721 167727 167729 167735 167739 167741 167745 167747 167751 167753 167755 167756 167757 167759 167760 167761 167763 167765 167769 167771 167775 167777 167781 167787 167789 167795 167799 167801 167805 167811 167817 167819 167825 167829 167831 167837 167841 167847 167855 203614
| A. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| B. | 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 | |
| C. | 在非金属元素区域可以寻找制备新型农药材料的元素 | |
| D. | 在地球上元素的分布和它们在元素周期表中的位置有密切关系 |
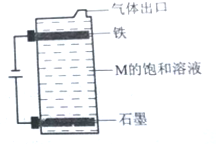 A、B、C、D、E为原子序数依次增大的短周期元素.A、C处于同一主族,C、D、E处于同一周期;A、B组成的气体X能使湿润的红色石蕊试纸变蓝.C在短周期元素中金属性最强,E原子的最外层电子数是A、B、C原子最外层电子数之和,E的单质与x反应能生成溶于水呈强酸性的化合物Z,同时生成B的单质,D的单质既能与C的最高价氧化物的水溶液反应,也能与Z的水溶液反应;C、E可组成化合物M.
A、B、C、D、E为原子序数依次增大的短周期元素.A、C处于同一主族,C、D、E处于同一周期;A、B组成的气体X能使湿润的红色石蕊试纸变蓝.C在短周期元素中金属性最强,E原子的最外层电子数是A、B、C原子最外层电子数之和,E的单质与x反应能生成溶于水呈强酸性的化合物Z,同时生成B的单质,D的单质既能与C的最高价氧化物的水溶液反应,也能与Z的水溶液反应;C、E可组成化合物M.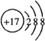 .
.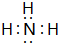 ;
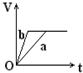
; 向足量的a、b两份锌粉中,分别加入少量且等量的稀H2SO4,同时向a中加入少量的CuSO4溶液.下图表示产生H2的体积(V)与时间(t)的关系,其中正确的是( )
向足量的a、b两份锌粉中,分别加入少量且等量的稀H2SO4,同时向a中加入少量的CuSO4溶液.下图表示产生H2的体积(V)与时间(t)的关系,其中正确的是( )