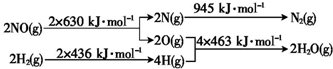
6.工业上由焦炭或天然气制氢气的过程中会产生一氧化碳.为了除去氢气中混有的一氧化碳,可在催化剂存在的条件下发生反应:
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.0kJ/mol
该反应在工业上被称为“一氧化碳变换”反应.
(1)在一个容积为1L的密闭容器中加入1molCO和3molH2O(g),发生上述反应,5min后达到平衡,测得该反应实际放出的热量为20.5kJ,迅速导出热量,保持容器中温度不变.则该时间范围内反应的平均速率ν(CO)=0.1mol/(L•min);平衡常数K的数值为0.2.
(2)某工业合成氨的原料气组成为:H2 40%、N2 20%、CO 30%、CO210%(均为体积分数).
现采用“一氧化碳变换”法,向上述原料气中加入水蒸气,将其中的CO除去.已知不同温度
及反应物投料比($\frac{n({H}_{2}O)}{n(CO)}$)下,变换反应后平衡混合气体中CO的体积分数如下表所示:
①平衡混合气体中CO的体积分数越大,则CO的平衡转化率越小(填“大”或“小”).
②从该反应的化学方程式分析,反应物投料比($\frac{n({H}_{2}O)}{n(CO)}$)越大,CO的平衡转化率越大(填
“大”或“小”),与上表中的数据分析结果相符(填“相符”或“不符”).根据对上表的分析,为提高CO平衡转化率,还可以采取的措施是降低温度.
③不同温度下该反应K值:K(300℃)<K(200℃)(填“>”、“=”或“<”).
④温度是一氧化碳变换工艺中最重要的条件,实际生产过程中将温度控制在300℃左右,其原因是升高温度,会提高反应速率,但平衡逆向移动,CO的平衡转化率下降,实际生产中应综合考虑速率和平衡两个方面.
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.0kJ/mol
该反应在工业上被称为“一氧化碳变换”反应.
(1)在一个容积为1L的密闭容器中加入1molCO和3molH2O(g),发生上述反应,5min后达到平衡,测得该反应实际放出的热量为20.5kJ,迅速导出热量,保持容器中温度不变.则该时间范围内反应的平均速率ν(CO)=0.1mol/(L•min);平衡常数K的数值为0.2.
(2)某工业合成氨的原料气组成为:H2 40%、N2 20%、CO 30%、CO210%(均为体积分数).
现采用“一氧化碳变换”法,向上述原料气中加入水蒸气,将其中的CO除去.已知不同温度
及反应物投料比($\frac{n({H}_{2}O)}{n(CO)}$)下,变换反应后平衡混合气体中CO的体积分数如下表所示:
| 温度/℃\CO的体积分数%\投料比 | $\frac{n({H}_{2}O)}{n(CO)}$=1 | $\frac{n({H}_{2}O)}{n(CO)}$=3 | $\frac{n({H}_{2}O)}{n(CO)}$=5 |
| 200 250 300 350 | 1.70 2.73 6.00 7.85 | 0.21 0.30 0.84 1.52 | 0.02 0.06 0.43 0.80 |
②从该反应的化学方程式分析,反应物投料比($\frac{n({H}_{2}O)}{n(CO)}$)越大,CO的平衡转化率越大(填
“大”或“小”),与上表中的数据分析结果相符(填“相符”或“不符”).根据对上表的分析,为提高CO平衡转化率,还可以采取的措施是降低温度.
③不同温度下该反应K值:K(300℃)<K(200℃)(填“>”、“=”或“<”).
④温度是一氧化碳变换工艺中最重要的条件,实际生产过程中将温度控制在300℃左右,其原因是升高温度,会提高反应速率,但平衡逆向移动,CO的平衡转化率下降,实际生产中应综合考虑速率和平衡两个方面.
5.在一定温度下,将气体X和气体Y各0.16mol充入10L 恒容密闭容器中,发生反应:X(g)+Y(g)═2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2min的平均速率ν(Z)=2.0×10-5 mol/(L•min) | |
| B. | 4min时,ν(逆)>ν(正) | |
| C. | 该温度下,此反应的平衡常数K=1.44 | |
| D. | 7min时,反应还未达到平衡状态 |
3.已知:2CH3OH(g)?CH3OCH3(g)+H2O(g);△H=-25kJ•mol-1,某温度下的平衡常数为400.此温度下,在1L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下表,下列说法正确的是( )
| 物质 | CH3OH | CH3OCH3 | H2O |
| c/(mol•L-1) | 0.8 | 1.24 | 1.24 |
| A. | 平衡后升高温度,平衡常数>400 | |
| B. | 平衡时,c(CH3OCH3)=1.6 mol•L-1 | |
| C. | 平衡时,反应混合物的总能量减少40 kJ | |
| D. | 平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大 |
19.对于化学反应A(g)+3B(g)?3C(g),下列措施既可加快反应速度,有可提高A的转化率的是( )
| A. | 使用催化剂 | B. | 增大A物质的浓度 | C. | 增大B物质的浓度 | D. | 减少C物质的浓度 |
18.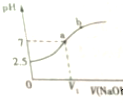 常温下,在10mL 0.1mol•L-1 NaHSO3溶液中逐滴滴加0.1mol•L-1 NaOH溶液,反应过程中溶液pH变化如图所示,下列说法不正确的是( )
常温下,在10mL 0.1mol•L-1 NaHSO3溶液中逐滴滴加0.1mol•L-1 NaOH溶液,反应过程中溶液pH变化如图所示,下列说法不正确的是( )
0 167316 167324 167330 167334 167340 167342 167346 167352 167354 167360 167366 167370 167372 167376 167382 167384 167390 167394 167396 167400 167402 167406 167408 167410 167411 167412 167414 167415 167416 167418 167420 167424 167426 167430 167432 167436 167442 167444 167450 167454 167456 167460 167466 167472 167474 167480 167484 167486 167492 167496 167502 167510 203614
 常温下,在10mL 0.1mol•L-1 NaHSO3溶液中逐滴滴加0.1mol•L-1 NaOH溶液,反应过程中溶液pH变化如图所示,下列说法不正确的是( )
常温下,在10mL 0.1mol•L-1 NaHSO3溶液中逐滴滴加0.1mol•L-1 NaOH溶液,反应过程中溶液pH变化如图所示,下列说法不正确的是( )| A. | NaHSO3溶液呈酸性 | B. | V1<10mL | ||
| C. | 在a点,c(Na+)=c(SO32- )+c(HSO3-) | D. | HSO3-的电离常数Ka=6.25×10-7 |
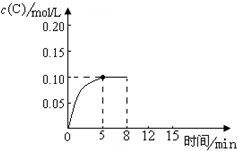 在500℃时,将足量的A固体投入2.0L真空密闭容器中,发生A(s)═2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示
在500℃时,将足量的A固体投入2.0L真空密闭容器中,发生A(s)═2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示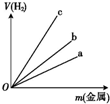 氢是一种重要的非金属元素.氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用.
氢是一种重要的非金属元素.氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用.