7.最近,美国科学家宣布其发现的二种超重新元素是错误的;俄罗斯科学家则宣布发现了114号超重新元素,其相对原子质量为289,质子数为114.下列说法正确的是( )
| A. | 114号元素原子的中子数为175 | |
| B. | 114号元素原子的中子数为403 | |
| C. | 科学家宣布自己的研究成果错误是可耻的 | |
| D. | 科学研究成果是不可能有错误的 |
6.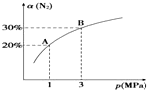 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )
 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )| A. | 将1 mol氮气、3 mol氢气,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ | |
| B. | 平衡状态由A变到B时,平衡常数K(A)<K(B) | |
| C. | 上述反应在达到平衡后,增大压强,H2的转化率增大 | |
| D. | 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小 |
5.某恒温密闭容器中,可逆反应A(s)?B+C(g)-Q达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )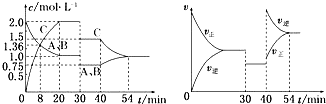

| A. | 产物B的状态只能为固态或液态 | |
| B. | 平衡时,单位时间内n(A)消耗:n(C)消耗=1:1 | |
| C. | 保持体积不变,向平衡体系中加入A,平衡向正反应方向移动 | |
| D. | 若开始时向容器中加入1 mol B和1 mol C,达到平衡时放出热量Q |
4.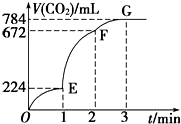 用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积),下列分析正确的是( )
用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积),下列分析正确的是( )
 用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积),下列分析正确的是( )
用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积),下列分析正确的是( )| A. | OE段表示的平均速率最快 | |
| B. | EF段,用盐酸表示该反应的平均反应速率为0.4 mol•L-1•min-1 | |
| C. | OE、EF、FG三段中,该反应用二氧化碳表示的平均反应速率之比为2:6:7 | |
| D. | F点收集到的CO2的量最多 |
1.如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得两端导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )

| A. | 产生气体的体积:①>② | |
| B. | 两极上析出物质的质量:①>② | |
| C. | 溶液的pH变化:①增大,②减小 | |
| D. | 电极反应式:①中阳极:4OH--→2H2O+O2↑+4e-;②中阴极:2H++2e--→H2↑ |
20.下列离子方程式不正确的是( )
| A. | 用碳酸钠溶液吸收少量二氧化硫:2 CO32-+SO2+H2O=2 HCO3-+SO32- | |
| B. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液使SO42-沉淀完全:2Ba2++NH4++Al3++2 SO42-+4OH-=Al(OH)3↓+2BaSO4↓+NH3•H2O | |
| C. | 0.5mol/L的NaHSO3溶液与1.0mol/L的NaClO溶液等体积混合:HSO3-+ClO-=SO42-+Cl-+H+ | |
| D. | 将1 mol/L NaAlO2溶液和1.5 mol/L HCl溶液等体积互相均匀混合:6 AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ |
18.将5mol/L MgCl2溶液a mL稀释至b mL,稀释后溶液中Cl-的物质的量浓度为( )
0 167169 167177 167183 167187 167193 167195 167199 167205 167207 167213 167219 167223 167225 167229 167235 167237 167243 167247 167249 167253 167255 167259 167261 167263 167264 167265 167267 167268 167269 167271 167273 167277 167279 167283 167285 167289 167295 167297 167303 167307 167309 167313 167319 167325 167327 167333 167337 167339 167345 167349 167355 167363 203614
| A. | $\frac{5a}{b}$ mol/L | B. | $\frac{10a}{b}$ mol/L | C. | $\frac{b}{5a}$ mol/L | D. | $\frac{a}{b}$ mol/L |
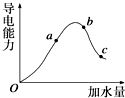 一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答: .
.