4.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑦七种元素在周期表中的位置.
请回答:
(1)下列元素分别是①Na(填元素符号,下同),其中化学性质最不活泼的是Ar.
(2)⑥元素的氢化物是 (填电子式),该氢化物在常温下与②发生反应的化学方程式为2K+2H2O=2KOH+H2↑.
(填电子式),该氢化物在常温下与②发生反应的化学方程式为2K+2H2O=2KOH+H2↑.
(3)⑦元素与①元素形成的化合物是NaC(填化学式),高温下灼烧该化合物时,火焰呈黄色.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑦ | ④ | ||||
| 4 | ② |
(1)下列元素分别是①Na(填元素符号,下同),其中化学性质最不活泼的是Ar.
(2)⑥元素的氢化物是
 (填电子式),该氢化物在常温下与②发生反应的化学方程式为2K+2H2O=2KOH+H2↑.
(填电子式),该氢化物在常温下与②发生反应的化学方程式为2K+2H2O=2KOH+H2↑.(3)⑦元素与①元素形成的化合物是NaC(填化学式),高温下灼烧该化合物时,火焰呈黄色.
3.一定温度下,在三个体积均为2.0L的恒容密闭容器中发生如下反应:
PCl5(g)?PCl3(g)+Cl2(g)
下列说法正确的是( )
PCl5(g)?PCl3(g)+Cl2(g)
| 编号 | 温度(℃) | 起始物质的量 (mol) | 平衡物质的量 (mol) | 达到平衡所需时间 (s) | |
| PCl5(g) | PCl3(g) | Cl2(g) | |||
| Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
| Ⅱ | 320 | 0.80 | t2 | ||
| Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
| A. | 平衡常数K:容器Ⅱ>容器Ⅲ | |
| B. | 反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ | |
| C. | 反应到达平衡时,容器I中的平均速率为v(PCl5)=$\frac{0.10}{{t}_{1}}$mol/(L•s) | |
| D. | 起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl30.45 mol和Cl20.10 mol,则反应将向逆反应方向进行 |
2.下列有关物质结构的表述正确的是( )
| A. | 次氯酸的电子式  | B. | 氯化钠的分子式 NaCl | ||
| C. | 硫原子的最外层电子排布式3s23p4 | D. | 钠离子的结构示意图 |
1.将Na2O2逐渐加入到含有Mg2+、NH4+的混合液中并微热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如下图所示,则原混合液中Al3+、Mg2+、NH4+的物质的量分别是( )
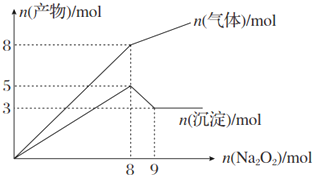

| A. | 2 mol、3 mol、4 mol | B. | 2 mol、3 mol、8 mol | ||
| C. | 3 mol、2 mol、8 mol | D. | 3 mol、2 mol、4 mol |
20.下列分子中,所有原子都满足最外层为8电子结构的是( )
| A. | H2O | B. | BF3 | C. | COCl2 | D. | SF6 |
19.下列化合物的电子式书写正确的是( )
| A. |  | B. |  | C. | 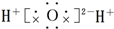 | D. | 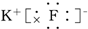 |
18.与OH-具有相同质子数和电子数的粒子是( )
| A. | F- | B. | NH3 | C. | H2O | D. | Na+ |
16.用金属铜制取硝酸铜,从节约原料和防止环境污染考虑,最好的方法是( )
| A. | 铜$\stackrel{浓硫酸}{→}$硝酸铜 | B. | 铜$\stackrel{稀硫酸}{→}$硝酸铜 | ||
| C. | Cu$\stackrel{Cl_{2}}{→}$CuCl2$\stackrel{AgNO_{3}}{→}$Cu(NO3)2 | D. | Cu$\stackrel{空气}{→}$CuO$\stackrel{HNO_{3}}{→}$Cu(NO3)2 |
15.下列说法不正确的是( )
0 167009 167017 167023 167027 167033 167035 167039 167045 167047 167053 167059 167063 167065 167069 167075 167077 167083 167087 167089 167093 167095 167099 167101 167103 167104 167105 167107 167108 167109 167111 167113 167117 167119 167123 167125 167129 167135 167137 167143 167147 167149 167153 167159 167165 167167 167173 167177 167179 167185 167189 167195 167203 203614
| A. | 0.1mol/L硫酸铵溶液中各离子的浓度由大到小的顺序是:c (NH4+)>c(SO42-)>c(H+)>c(OH-) | |
| B. | 在苏打与小苏打的混合溶液中存在:c(Na+)+c(H+)=c(OH -)+2c(CO32-)+c(HCO3-) | |
| C. | 在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,证明Na2CO3溶液中存在水解平衡 | |
| D. | 常温常压下能自发进行的反应,一定都是放热反应 |