题目内容
TiO2既是制备其他含钛化合物的原料,又是一种性能优异的白色颜料。
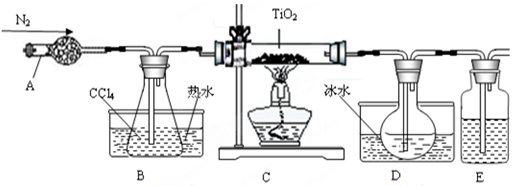
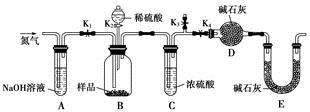
(1)实验室利用反应TiO2(s)+2CCl4(g)=TiCl4(g)+CO2(g),在无水无氧条件下,制取TiCl4实验装置示意图如下:
有关性质如下表
仪器A的名称是 ,装置E中的试剂是 。反应开始前依次进行如下操作:组装仪器、 、加装药品、通N2一段时间后点燃酒精灯。反应结束后的操作包括:①停止通氮气②熄灭酒精灯③冷却至室温。正确的顺序为 (填序号)。欲分离D中的液态混合物,所采用操作的名称是 。
(2)工业上由钛铁矿(FeTiO3)(含Fe2O3、SiO2等杂质)制备TiO2的有关反应包括:
酸溶FeTiO3(s)+2H2SO4(aq)=FeSO4(aq)+ TiOSO4(aq)+ 2H2O(l)
水解TiOSO4(aq)+ 2H2O(l)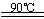 H2TiO3(s)+H2SO4(aq)
H2TiO3(s)+H2SO4(aq)
简要工艺流程如下:
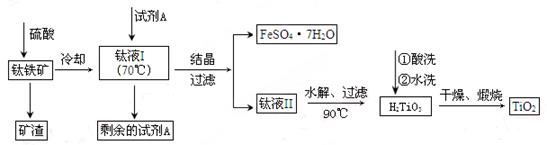
①试剂A为 。钛液Ⅰ需冷却至70℃左右,若温度过高会导致产品收率降低,原因是 。
②取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是 。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2也会发黄,发黄的杂质是 (填化学式)。
(1)实验室利用反应TiO2(s)+2CCl4(g)=TiCl4(g)+CO2(g),在无水无氧条件下,制取TiCl4实验装置示意图如下:

有关性质如下表
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
(2)工业上由钛铁矿(FeTiO3)(含Fe2O3、SiO2等杂质)制备TiO2的有关反应包括:
酸溶FeTiO3(s)+2H2SO4(aq)=FeSO4(aq)+ TiOSO4(aq)+ 2H2O(l)
水解TiOSO4(aq)+ 2H2O(l)
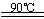 H2TiO3(s)+H2SO4(aq)
H2TiO3(s)+H2SO4(aq)简要工艺流程如下:

①试剂A为 。钛液Ⅰ需冷却至70℃左右,若温度过高会导致产品收率降低,原因是 。
②取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是 。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2也会发黄,发黄的杂质是 (填化学式)。
(1)干燥管;浓硫酸;检查气密性;②③①,分液(或蒸馏)
(2)①Fe 温度过高会导致TiSO4提前水解,产生H2SiO3沉淀
②Fe2+,Fe2O3
(2)①Fe 温度过高会导致TiSO4提前水解,产生H2SiO3沉淀
②Fe2+,Fe2O3
(1)仪器A是干燥管,由于IiCl4遇到水蒸气会水解,所以E中用浓硫酸吸收空气中水蒸气。对于气体制取而言,组装仪器、检查气密性、加药品,终止实验时防止倒吸,应先熄灭酒精灯,冷却到室温后再停止通入N2。分离两种沸点不同的液体混合物应该用蒸馏法。
(2)①矿石经硫酸溶解后得到的Fe2(SO4)3,而后过滤得到的是FeSO4·7H2O,所以试剂A是铁粉,把Fe3+还原为Fe2+。因为TiOSO4容易水解,若温度过高,则会有较多TiOSO4水解为固体H2TiO3,而经过滤进入FeSO4·7H2O中导致TiO2产率降低。
②加入KSCN溶液无现象,加H2O2出现红色,说明存在Fe2+,经过加热后Fe2+氧化为Fe2O3,而使产品发黄。
(2)①矿石经硫酸溶解后得到的Fe2(SO4)3,而后过滤得到的是FeSO4·7H2O,所以试剂A是铁粉,把Fe3+还原为Fe2+。因为TiOSO4容易水解,若温度过高,则会有较多TiOSO4水解为固体H2TiO3,而经过滤进入FeSO4·7H2O中导致TiO2产率降低。
②加入KSCN溶液无现象,加H2O2出现红色,说明存在Fe2+,经过加热后Fe2+氧化为Fe2O3,而使产品发黄。

练习册系列答案
相关题目
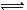 NH2COONH4(s) ΔH<0
NH2COONH4(s) ΔH<0 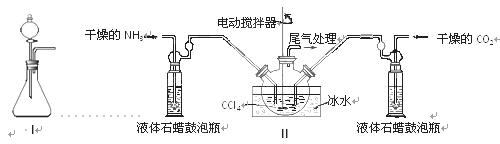

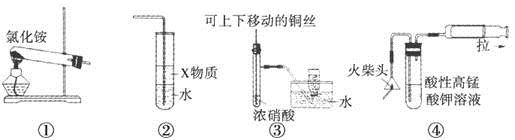
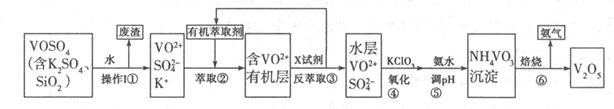
 2RAn(有机层)+nH2SO4(水层),
2RAn(有机层)+nH2SO4(水层),