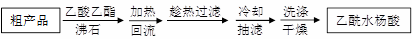题目内容
银氨溶液可用于检测CO气体。实验室研究该反应的装置图如下:
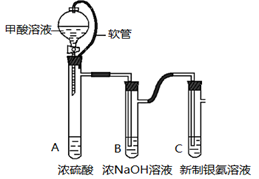
(1)甲酸在浓硫酸条件下能分解生成CO和H2O,体现浓硫酸具有 (填“氧化性”或脱水性)。
(2)软管的作用是 。
(3)浓NaOH溶液的作用是 。
(4)反应结束后试管C底部有黑色沉淀,为验证产物,分离出上层清液和底部黑色固体,并进行实验。
a.测得上层清液pH为10。
b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润红色石蕊试纸变蓝的气体。
c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象。
d.将黑色沉淀用蒸馏水洗净。
① 实验c的目的是 。
② 根据上述实验现象证明上层清液中含有 。
③ 已知银可溶于浓硝酸,设计实验证明黑色固体是Ag单质:
④ CO与银氨溶液反应中有氨气生成,根据实验现象写出该反应的化学方程式: 。

(1)甲酸在浓硫酸条件下能分解生成CO和H2O,体现浓硫酸具有 (填“氧化性”或脱水性)。
(2)软管的作用是 。
(3)浓NaOH溶液的作用是 。
(4)反应结束后试管C底部有黑色沉淀,为验证产物,分离出上层清液和底部黑色固体,并进行实验。
a.测得上层清液pH为10。
b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润红色石蕊试纸变蓝的气体。
c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象。
d.将黑色沉淀用蒸馏水洗净。
① 实验c的目的是 。
② 根据上述实验现象证明上层清液中含有 。
③ 已知银可溶于浓硝酸,设计实验证明黑色固体是Ag单质:
④ CO与银氨溶液反应中有氨气生成,根据实验现象写出该反应的化学方程式: 。
(1)脱水性 (2)保证分液漏斗和试管A内气压相同使甲酸溶液可以顺利滴下。
(3)洗气,吸收酸性气体
(4)①对比试验,证明Ba(OH)2溶液不能与银氨溶液反应,证明实验b中的现象是产物与Ba(OH)2溶液反应导致的。②(NH4)2CO3或NH4+、CO32—。③取少量黑色固体,向其中滴加浓硝酸,固体全部溶解并有少量红棕色气体产生,继续滴加NaCl 溶液,能产生白色沉淀,说明黑色固体为单质银。CO+ 2Ag(NH3)2OH=(NH4)2CO3+2Ag↓+2NH3↑
(3)洗气,吸收酸性气体
(4)①对比试验,证明Ba(OH)2溶液不能与银氨溶液反应,证明实验b中的现象是产物与Ba(OH)2溶液反应导致的。②(NH4)2CO3或NH4+、CO32—。③取少量黑色固体,向其中滴加浓硝酸,固体全部溶解并有少量红棕色气体产生,继续滴加NaCl 溶液,能产生白色沉淀,说明黑色固体为单质银。CO+ 2Ag(NH3)2OH=(NH4)2CO3+2Ag↓+2NH3↑
试题分析:(1)甲酸与浓硫酸共热发生反应:HCOOH
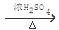 CO↑+H2O。在该反应中浓硫酸的作用是脱水性。(2)软管的作用是使分液漏斗的上下气体压强相同,这样分液漏斗中的液体在重力的作用下就可以顺利滴下。(3)甲酸在加热时会挥发,也可能部分CO被氧化为CO2,所以浓NaOH溶液的作用是洗气,吸收酸性气体。(4)a.测得上层清液pH为10,证明溶液为碱性;b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润红色石蕊试纸变蓝的气体。证明含有NH4+;同时证明在溶液中含有的离子能与Ba(OH)2电离产生的离子结合形成白色难溶性物质。根据反应物及所含元素可确定产生的白色沉淀为BaCO3。c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象。d.CO被银氨溶液氧化为CO32—,它本身则被还原为Ag单质。疏松的Ag颗粒在室温下为黑色固体。将黑色沉淀用蒸馏水洗净就得到单质Ag。① 实验c的目的是是为了与b形成对照,证明Ba(OH)2溶液不能与银氨溶液反应,实验b中的现象是产物与Ba(OH)2溶液反应导致的。② 根据上述实验现象证明上层清液中含有(NH4)2CO3或NH4+、CO32—。③证明黑色固体是Ag单质实验方案是取少量黑色固体,向其中滴加浓硝酸,固体全部溶解并有少量红棕色气体产生,继续滴加NaCl 溶液,能产生白色沉淀,说明黑色固体为单质银。④根据实验现象可知CO与银氨溶液反应的化学方程式为CO+ 2Ag(NH3)2OH=(NH4)2CO3+2Ag↓+2NH3↑。
CO↑+H2O。在该反应中浓硫酸的作用是脱水性。(2)软管的作用是使分液漏斗的上下气体压强相同,这样分液漏斗中的液体在重力的作用下就可以顺利滴下。(3)甲酸在加热时会挥发,也可能部分CO被氧化为CO2,所以浓NaOH溶液的作用是洗气,吸收酸性气体。(4)a.测得上层清液pH为10,证明溶液为碱性;b.向上层清液中滴加几滴Ba(OH)2溶液,发现有白色浑浊出现,同时产生能使湿润红色石蕊试纸变蓝的气体。证明含有NH4+;同时证明在溶液中含有的离子能与Ba(OH)2电离产生的离子结合形成白色难溶性物质。根据反应物及所含元素可确定产生的白色沉淀为BaCO3。c.取新制的银氨溶液滴加几滴Ba(OH)2溶液,无明显现象。d.CO被银氨溶液氧化为CO32—,它本身则被还原为Ag单质。疏松的Ag颗粒在室温下为黑色固体。将黑色沉淀用蒸馏水洗净就得到单质Ag。① 实验c的目的是是为了与b形成对照,证明Ba(OH)2溶液不能与银氨溶液反应,实验b中的现象是产物与Ba(OH)2溶液反应导致的。② 根据上述实验现象证明上层清液中含有(NH4)2CO3或NH4+、CO32—。③证明黑色固体是Ag单质实验方案是取少量黑色固体,向其中滴加浓硝酸,固体全部溶解并有少量红棕色气体产生,继续滴加NaCl 溶液,能产生白色沉淀,说明黑色固体为单质银。④根据实验现象可知CO与银氨溶液反应的化学方程式为CO+ 2Ag(NH3)2OH=(NH4)2CO3+2Ag↓+2NH3↑。
练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
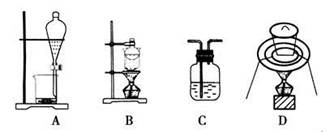
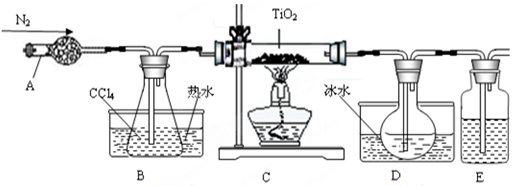
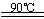 H2TiO3(s)+H2SO4(aq)
H2TiO3(s)+H2SO4(aq)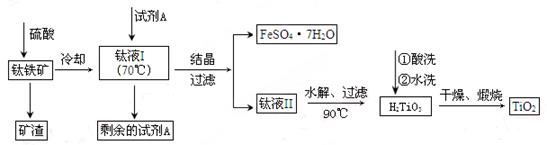
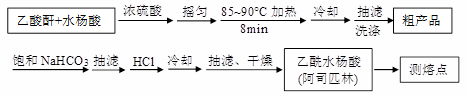
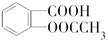 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下: