题目内容
12.下列化学用语表达不正确的是( )| A. | 乙烯的比例模型: | B. | 丙烷分子的球棍模型: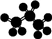 | ||
| C. | 醋酸钠的分子式:CH3COONa | D. | 乙酸的结构简式:CH3COOH |
分析 A.比例模型反应原子的大小,C原子比H原子大,黑色球表示C原子;
B.球棍模型突出的是原子之间的成键的情况及空间结构;
C.醋酸钠为离子晶体,不存在分子式,只能说是化学式;
D.乙酸由甲基与羧基构成.
解答 解:A.C原子比H原子大,黑色球表示C原子,则乙烯的比例模型为 ,故A正确;
,故A正确;
B.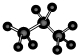 原子之间为单键,主链有3个碳原子,氢原子数为8个,符合丙烷的结构,故B正确;
原子之间为单键,主链有3个碳原子,氢原子数为8个,符合丙烷的结构,故B正确;
C.醋酸钠为离子晶体,不存在分子式,只能说是化学式,故C错误;
D.乙酸的分子式为:C2H4O2,结构简式为CH3COOH,故D正确;
故选C.
点评 本题考查化学用语,涉及比例模型、球棍模型、分子式、结构简式等,注意区分及规范使用化学用语,题目难度不大.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案
相关题目
14.物质M在水中发生如下电离:M=X2++2Y-,则下列判断正确的是( )
| A. | M一定不是酸 | B. | X2+一定是金属离子 | ||
| C. | Y-是OH- | D. | M是一定属于盐 |
3.下列各组混合物中,不论两种物质以何种比例混合,只要总质量一定,经过完全燃烧后,产生的CO2质量不变的是( )
| A. | 乙炔和甲苯 | B. | 丙烯和丙烷 | C. | 乙醇和丙酸 | D. | 甲醛与葡萄糖 |
20. 在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)?zC(g),图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是
在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)?zC(g),图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是
( )
 在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)?zC(g),图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是
在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)?zC(g),图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )
| A. | 200℃时,反应从开始到平衡的平均速率v(B)=0.04 mol•L-1•min-1 | |
| B. | 由图乙可知,反应xA(g)+yB(g)?zC(g)的△H<0,且a=2 | |
| C. | 若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数减小.达到平衡时,A的体积分数小于0.5 | |
| D. | 200℃时,起始向容器中充入0.2 mol A、0.4 mol B和0.4 mol C,反应达到平衡前的速率:v(正)<v(逆) |
7.取10g氢气和CH3OH的混合物在氧气中完全燃烧,将其产物和足量的过氧化钠反应,反应后固体的质量增加了( )
| A. | 9 g | B. | 10 g | C. | 11 g | D. | 12 g |
17.下列关于碳氢化合物的叙述正确的是( )
| A. | 碳氢化合物的通式都可以表示为CnH2n+2 | |
| B. | 燃烧产物为二氧化碳和水的化合物一定是碳氢化合物 | |
| C. | 含有碳碳单键的化合物都为烷烃 | |
| D. | 烃的相对分子质量一定是2的倍数 |
1.分子式为C9H12O,含有苯环的醇类同分异构体共有(不考虑立体异构)( )
| A. | 10种 | B. | 8种 | C. | 6种 | D. | 4种 |
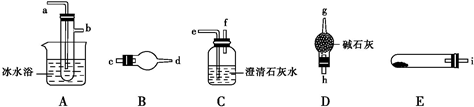
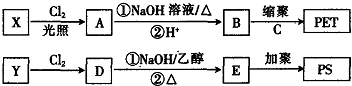
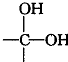 →
→
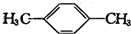 ,其核磁共振氢谱有2种峰.
,其核磁共振氢谱有2种峰. ,
, .
.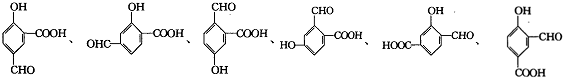 (其中一种).
(其中一种).