题目内容
(4分) 已知:
①P4(S,白磷)+5O2(g)= P4O10(S)△H = —2983.2kJ?mol-1
②P(S,红磷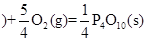 △H = —738.5kJ?mol-1
△H = —738.5kJ?mol-1
(1)写出白磷转化为红磷的热化学方程式: 。
(2)则对应下列化学反应过程中的能量变化图,能正确反映出由白磷转化为红磷的是[选填A ~ D] 。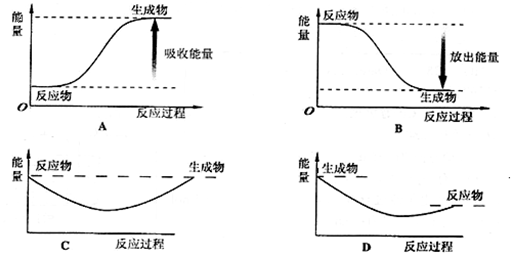
①P4(S,白磷)+5O2(g)= P4O10(S)△H = —2983.2kJ?mol-1
②P(S,红磷
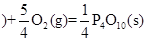 △H = —738.5kJ?mol-1
△H = —738.5kJ?mol-1(1)写出白磷转化为红磷的热化学方程式: 。
(2)则对应下列化学反应过程中的能量变化图,能正确反映出由白磷转化为红磷的是[选填A ~ D] 。

P4(s,白磷)= 4P(s,红磷) △H = —29.2kJ?mol-1(2分);B(2分)
(1)根据盖斯定律可知,①-②×4即得到P4(s,白磷)= 4P(s,红磷),所以该反应的反应热△H =—2983.2kJ?mol-1+738.5kJ?mol-1×4=—29.2kJ?mol-1。
(2)根据热化学方程式可知,白磷转化为红磷的反应是放热反应,这说明白磷的总能量高于红磷的总能量,因此图像B是正确的,答案选B。
(2)根据热化学方程式可知,白磷转化为红磷的反应是放热反应,这说明白磷的总能量高于红磷的总能量,因此图像B是正确的,答案选B。

练习册系列答案
相关题目
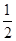 H2SO4(浓)+ NaOH(aq)=
H2SO4(浓)+ NaOH(aq)=
 2SO3;△H= —196.6 kJ/mol
2SO3;△H= —196.6 kJ/mol 2(t-BuNO),测得该反应的ΔH =" +50.5" kJ·mol-1,活化能Ea =" 90.4" kJ·mol-1。能量关系图合理的是
2(t-BuNO),测得该反应的ΔH =" +50.5" kJ·mol-1,活化能Ea =" 90.4" kJ·mol-1。能量关系图合理的是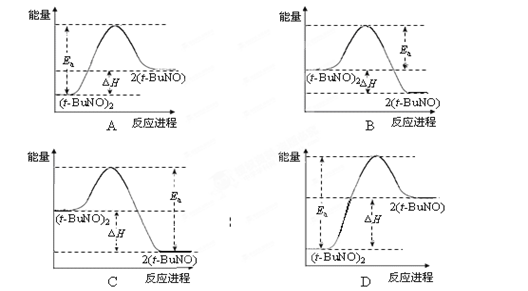
 2SO3(g) △H =" a" kJ·mol-1,反应过程的能量变化如图所示。已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ。请回答:
2SO3(g) △H =" a" kJ·mol-1,反应过程的能量变化如图所示。已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ。请回答: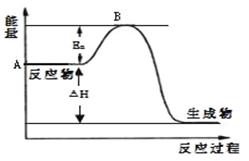
 CH3OH(g)+H2O(g),右图表示该反应进行过程中能量的变化。
CH3OH(g)+H2O(g),右图表示该反应进行过程中能量的变化。
