题目内容
15. 为维持人体血液中的血糖含量,在给病人输液时,通常用葡萄糖注射液.如图是医院病人输液使用的一瓶质量分数为6%的葡萄糖(C6H12O6)注射液标签,请认真观察标签上所列内容后计算:
为维持人体血液中的血糖含量,在给病人输液时,通常用葡萄糖注射液.如图是医院病人输液使用的一瓶质量分数为6%的葡萄糖(C6H12O6)注射液标签,请认真观察标签上所列内容后计算:(1)该溶液的物质的量浓度为0.5mol•L-1(精确到0.1g).
(2)该溶液的密度为1.5g•mL-1(精确到0.1g).
(3)如果从该瓶中取出75g葡萄糖注射液,将其变为15%的注射液,需要加入7.9g葡萄糖固体(精确到0.1g).
分析 (1)由图片信息可知,1L溶液中含有90g葡萄糖,根据n=$\frac{m}{M}$计算葡萄糖的物质的量,再根据c=$\frac{n}{V}$计算葡萄糖物质的量浓度;
(2)结合葡萄糖质量分数计算1L溶液质量,再根据ρ=$\frac{m}{V}$计算溶液密度;
(3)设需要加入葡萄糖质量为mg,根据质量分数表示出葡萄糖的质量,加入葡萄糖的质量+原溶液中葡萄糖质量=15%的注射液中葡萄糖的质量.
解答 解:(1)由图片信息可知,1L溶液中含有90g葡萄糖,葡萄糖的物质的量为$\frac{90g}{180g/mol}$=0.5mol,则葡萄糖物质的量浓度为$\frac{0.5mol}{1L}$=0.5mol/L,
故答案为:0.5mol/L;
(2)1L溶液质量为$\frac{90g}{6%}$=1500g,则溶液密度=$\frac{1500g}{1000mL}$=1.5g/mL,
故答案为:1.5;
(3)设需要加入葡萄糖质量为mg,则:
75g×6%+mg=(m+75)g×15%
解得m=7.9
故答案为:7.9.
点评 本题考查溶液浓度有关计算,涉及物质的量浓度、质量分数有关计算,难度不大,有利于基础知识的巩固.

练习册系列答案
相关题目
5.已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16,下列有关说法中错误的是( )
| A. | AgCl不溶于水,不能转化为AgI | |
| B. | 两种不溶物的Ksp相差越小,不溶物就越容易转化为更难溶的不溶物 | |
| C. | AgI比AgCl更难溶于水,所以AgCl可以转化为AgI | |
| D. | 一定温度下,向AgCl的饱和溶液中加入NaCl固体,有AgCl固体析出 |
10.阿伏加德罗常数为6.02×1023 mol-1.下列叙述中正确的是( )
| A. | 标准状况下,2.24L煤油(设为C8H18)中含有4.816×1023个碳原子 | |
| B. | 常温常压下,O2和O3的混合物16g中含有6.02×1023个氧原子 | |
| C. | 25℃时,1L 0.1mol•L-1的氢氧化钠溶液中含有6.02×1023个OH- | |
| D. | 0.5mol CH4中含有3.01×1023个电子 |
20.下列关于反应速率的说法正确的是( )

| A. | 决定反应速率的主要因素是反应物的浓度 | |
| B. | 化学反应速率为0.8 mol/(L•s) 是指1s 时某物质的浓度为0.8mol/L | |
| C. | 用不同物质的浓度变化表示同一时间内、同一反应的速率时,其数值之比等于反应方程式中对应物质的化学计量数之比 | |
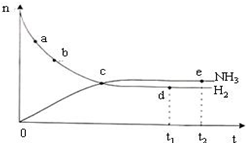
| D. | 如图表示密闭容器中673 K,30 MPa下的反应:N2(g)+3H2(g)?2NH3(g)△H<0,n(NH3)和n(H2)随时间变化的关系曲线图.点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
7.已知U、V、W、X、Y、Z均为元素周期表中前36号元素,且原子序数依次增大.U、V、W和X、Y分别为同一周期的主族元素,V原子p能级电子总数与s能级电子总数相等.U、Z原子中未成对电子数是同周期中最多的,且基态Z原子核外电子数是基态V原子核外电子数的3倍.X和Y原子的第一至第四电离能如表所示:
(1)试比较U、V、W三种元素电负性F>O>N(用元素符号填空),X、Y两元素中X的第一电离能较大的原因是原子价电子排布为3s2,而Al原子的价电子排布为3s23p1,Mg原子3s轨道全充满,3p轨道全空相对稳定
(2)基态Z原子的核外电子排布式为[Ar]3d54s1.该基态原子共有24种不同运动状态的电子.
(3)试写出U元素单质的2种等电子体,①CO,②CN-.
(4)将W的单质通入NaOH溶液中可得到VW2.VW2是一种无色、几乎无味的剧毒气体,主要用于氧化反应,火箭工程、助燃剂等.
①VW2中V原子的杂化轨道类型是sp3,VW2分子的空间构型为V形.
②与H2O分子相比,VW2分子的极性更小(填“大”或“小”),原因是F的电负性大于O,导致正负电荷中心偏离程度减小.
(5)金属Z内部原子的堆积方式与Na相同,都是体心立方堆积方式.则晶胞中Z的配位数为8,若该晶胞的边长为289pm,NA取值为6.02×1023,Z原子的摩尔质量为52g/mol,则Z的密度为7.1g/cm3.Z原子与次近的Z原子的核间距离为289pm.
| 电离能/kJ/mol | I1 | I2 | I3 | I4 |
| X | 738 | 1451 | 7733 | 10540 |
| Y | 578 | 1817 | 2745 | 11575 |
(2)基态Z原子的核外电子排布式为[Ar]3d54s1.该基态原子共有24种不同运动状态的电子.
(3)试写出U元素单质的2种等电子体,①CO,②CN-.
(4)将W的单质通入NaOH溶液中可得到VW2.VW2是一种无色、几乎无味的剧毒气体,主要用于氧化反应,火箭工程、助燃剂等.
①VW2中V原子的杂化轨道类型是sp3,VW2分子的空间构型为V形.
②与H2O分子相比,VW2分子的极性更小(填“大”或“小”),原因是F的电负性大于O,导致正负电荷中心偏离程度减小.
(5)金属Z内部原子的堆积方式与Na相同,都是体心立方堆积方式.则晶胞中Z的配位数为8,若该晶胞的边长为289pm,NA取值为6.02×1023,Z原子的摩尔质量为52g/mol,则Z的密度为7.1g/cm3.Z原子与次近的Z原子的核间距离为289pm.
4.能判断CO2为酸性氧化物的依据是( )
| A. | CO2+H2O═H2CO3 | B. | C+O2═CO2 | ||
| C. | CO2+2KOH═K2CO3+H2O | D. | CaO+CO2═CaCO3 |
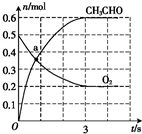 100℃时,在容积为2.0L的恒容密闭容器中,通入乙烯和氧气,其中乙烯和氧气物质的量之比为2:1,发生反应:2C2H4 (g)+O2(g)?2CH3CHO(g)△H<0,体系中部分物质的物质的量随时间变化如图所示.
100℃时,在容积为2.0L的恒容密闭容器中,通入乙烯和氧气,其中乙烯和氧气物质的量之比为2:1,发生反应:2C2H4 (g)+O2(g)?2CH3CHO(g)△H<0,体系中部分物质的物质的量随时间变化如图所示.