题目内容
18.下列转化关系中的A-E均为有机物(部分反应条件和产物已略去),其中PLA是一种可降解的了绿色分子材料,E为高分子化合物E可,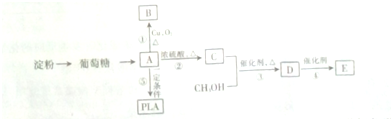
已知:A与葡萄糖的实验式相同,经质谱法检测A的式子量为90,其核磁共振氢谱显示有面积比为3:1:1:1的四个峰,请回答:
(1)A的结构简式为
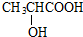 C中所含官能团的名称是羧基、碳碳双键
C中所含官能团的名称是羧基、碳碳双键(2)反应①的化学方程式为2
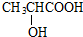 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$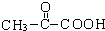 +2H2O反应④的化学方程式为n CH2=CHCOOCH3$\stackrel{催化剂}{→}$
+2H2O反应④的化学方程式为n CH2=CHCOOCH3$\stackrel{催化剂}{→}$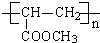
(3)反应②和③的反应类型分别是消去反应和酯化反应
(4)反应⑤的化学方程式为n
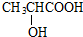 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ +(n-1)H2O
+(n-1)H2O(5)A有多种同分异构体,请写出分子中只含有两种不同环境氢原子的同分异构体的结构简式(任写两种)
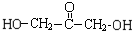 、
、 .
.
分析 淀粉水解得到葡糖糖,葡糖糖转化得到A,A与葡萄糖的实验式相同,则A的实验式为CH2O,经质谱法检测A的式子量为90,令A的分子组成为(CH2O)Hn,则30n=90,故n=3,则A的分子式为C3H6O3,A在Cu/氧气、加热条件下发生氧化反应生成B,则A中含有-OH,A在浓硫酸、加热条件下生成C,C能与甲醇反应,则A、C中含有-COOH,A核磁共振氢谱显示有面积比为3:1:1:1的四个峰,则A为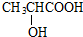 ,B为
,B为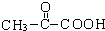 ,C为CH2=CHCOOH,D为CH2=CHCOOCH3,PLA是一种可降解的了绿色分子材料,则A发生缩聚反应生成PLA,故PLA的结构简式为
,C为CH2=CHCOOH,D为CH2=CHCOOCH3,PLA是一种可降解的了绿色分子材料,则A发生缩聚反应生成PLA,故PLA的结构简式为 ,D发生加聚反应生成高分子化合物E为
,D发生加聚反应生成高分子化合物E为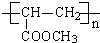 ,据此解答.
,据此解答.
解答 解:淀粉水解得到葡糖糖,葡糖糖转化得到A,A与葡萄糖的实验式相同,则A的实验式为CH2O,经质谱法检测A的式子量为90,令A的分子组成为(CH2O)Hn,则30n=90,故n=3,则A的分子式为C3H6O3,A在Cu/氧气、加热条件下发生氧化反应生成B,则A中含有-OH,A在浓硫酸、加热条件下生成C,C能与甲醇反应,则A、C中含有-COOH,A核磁共振氢谱显示有面积比为3:1:1:1的四个峰,则A为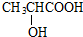 ,B为
,B为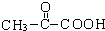 ,C为CH2=CHCOOH,D为CH2=CHCOOCH3,PLA是一种可降解的了绿色分子材料,则A发生缩聚反应生成PLA,故PLA的结构简式为
,C为CH2=CHCOOH,D为CH2=CHCOOCH3,PLA是一种可降解的了绿色分子材料,则A发生缩聚反应生成PLA,故PLA的结构简式为 ,D发生加聚反应生成高分子化合物E为
,D发生加聚反应生成高分子化合物E为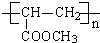 .
.
(1)由上述分析可知,A的结构简式为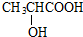 ,C为CH2=CHCOOH,所含官能团有:羧基、碳碳双键;
,C为CH2=CHCOOH,所含官能团有:羧基、碳碳双键;
故答案为: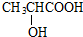 ;羧基、碳碳双键;
;羧基、碳碳双键;
(2)反应①的化学方程式为:2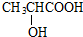 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$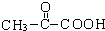 +2H2O,
+2H2O,
反应④的化学方程式为:n CH2=CHCOOCH3$\stackrel{催化剂}{→}$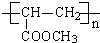 ,
,
故答案为:2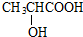 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$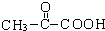 +2H2O;n CH2=CHCOOCH3$\stackrel{催化剂}{→}$
+2H2O;n CH2=CHCOOCH3$\stackrel{催化剂}{→}$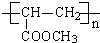 ;
;
(3)反应②属于消去反应,反应③属于酯化反应,故答案为:消去反应;酯化反应;
(4)反应⑤的化学方程式为:n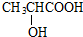 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ +(n-1)H2O,
+(n-1)H2O,
故答案为:n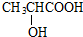 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ +(n-1)H2O;
+(n-1)H2O;
(5)A(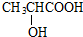 )有多种同分异构体,分子中只含有两种不同环境氢原子的同分异构体的结构简式有:
)有多种同分异构体,分子中只含有两种不同环境氢原子的同分异构体的结构简式有: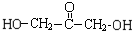 、
、 ,
,
故答案为: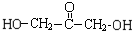 、
、 .
.
点评 本题考查有机物推断,计算确定A的分子式,再结合转化关系确定A含有的官能团,进而确定A的结构简式,需要学生熟练掌握官能团的性质与转化,难度中等.

 阅读快车系列答案
阅读快车系列答案反应①aRO3-+bI-+cH+=dR-+eI2+fH2O
反应②I2+2Na2S2O3=2NaI+Na2S4O6
下列说法正确的是( )
| A. | b=c | |
| B. | R元素位于周期表的ⅤA族 | |
| C. | 滴定终点时,溶液的颜色由无色变为蓝色 | |
| D. | 若滴定消耗Na2S2O3溶液20.00mL,则反应①转移电子6.02×1020个 |
| A. | 原子半径:W>Z>Y>X>M | |
| B. | 将XZ2通入W单质与水反应后的溶液中,生成的盐一定只有一种 | |
| C. | 由X、Y、Z、M四种元素共同形成的化合物中一定有共价键可能有离子键 | |
| D. | CaX2、CaM2、和CaZ2等3种化合物中,阳离子与阴离子个数比均为1:2 |
| 选项 | 叙述 | 结论 |
| A | 由次氯酸可制得盐酸 | 酸性:HClO>HCl |
| B | 原电池中负极金属的活动性,比正极强 | 镁、铝作电极与NaOH溶液组成原电池时,镁作负极 |
| C | -OH可与Na反应生成H2 | 可通过加钠凝聚是否具有气泡产生的方法鉴别乙醇的水溶液和乙酸的水溶液 |
| D | 溶解度小的沉淀易向更小的沉淀转化 | 向AgCl悬浊液中滴加KI溶液可得到AgI沉淀 |
| A. | A | B. | B | C. | C | D. | D |
| A. | Li | B. | S | C. | Li2S | D. | Li和S |
| A. | 新制生石灰 | B. | 新制氢氧化铜 | C. | 浓溴水 | D. | 银氨溶液 |
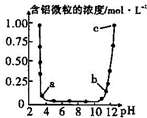 维持温度不变,向一定物质的量浓度的某AlCl3溶液中加入NaOH固体,忽略溶液体积的变化,溶液的pH与溶液中含铝微粒的物质的量浓度的关系如图.以下说法中正确的是( )
维持温度不变,向一定物质的量浓度的某AlCl3溶液中加入NaOH固体,忽略溶液体积的变化,溶液的pH与溶液中含铝微粒的物质的量浓度的关系如图.以下说法中正确的是( )| A. | a点表示溶液中的Al3+开始转化为Al(OH)3沉淀 | |
| B. | 据图可知,配制一定物质的量浓度的AlCl3溶液时,需要加入适量的H2SO4溶液抑制水解 | |
| C. | 当溶液的pH在6至8之间,铝元素全部以Al(OH)3的形式存在 | |
| D. | b点所对应的溶液中主要含铝微粒的水解程度大于c点 |
| 选项 | 现象或事实 | 解释 |
| A | 热的纯碱溶液去油污效果 更好 | 温度升高,增大了油脂在碳 酸钠溶液中的溶解度 |
| B | 生活中的铝制品经久耐用 | 常温时铝不与氧气反应 |
| C | 氢氧化铁胶体通直流电,阴极颜色变深 | 氛氧化铁胶体带正电荷,在电场力的作用下,胶体向阴极迁移 |
| D | 二氧化破用作通讯光缆 | 二氧化硅对光信号有良好的 传输性能 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 含氧酸的酸性:H3ZO4>H2YO4>HXO4 | |
| B. | 非金属性:X>Y>Z | |
| C. | 气态氢化物的稳定性按X、Y、Z顺序由弱到强 | |
| D. | 元素的负化合价的绝对值按X、Y、Z顺序由小到大 |