��Ŀ����
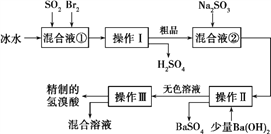
����Ŀ����ij��ͭ��ʯ[��Ҫ�ɷ���FeCuSi3O13(OH)4��������SiO2��CaCO3]Ϊԭ���Ʊ�CuSO4��5H2O���������£�

��֪����Լ��ɷֺͼ۸����±���ʾ��

��ش��������⣺
��1����ͭ��ʯ�����Ŀ����_______��
��2����������Һ�г���Cu2+�⣬�����еĽ�����������_______��
��3������1����NaOH��Һ�����ӷ���ʽΪ__________��
��4�����������Ϣ��֪����ѡ�õ��Լ�1������Ϊ_______��������Լ�ʱ��������Ӧ�����ӷ���ʽΪ_________��
��5���Լ�2 ����ѡ����������е�______������2��һ�����е�����Ϊ______(�ѧʽ����
A. Cu B.CuO C.Cu(OH)2 D.Fe
��6��CuSO4��5H2O���ڵ�⾫��ͭʱ��������ͨ��9.632��103C�ĵ�������������ܽ��ͭΪ16.0g�����������Һ��ԭ��ҺΪ1 L����ǡ����CuSO4����������������������_____g��ԭ���Һ��CuSO4��Ũ��Ϊ__ ����֪һ�����ӵĵ���Ϊ1.6��10-19C��
���𰸡� ��ߺ�ͭ��ʯ�������ʼ����Ч�� Fe2+ SiO2+2OH-=SiO32-+H2O ƯҺ ClO-+2Fe2++2H+=Cl-+2Fe3++H2O BC Fe(OH)3 32.0 0.25mol/L
����������ʯ�����������ϡ���ᷴӦ����ͭ��ת��Ϊ�����Σ����������̼��Ʊ�Ϊ����1�������ڸ����·�Ӧת��Ϊ����ƣ�Ҫ�õ�����ͭ������Ҫ��ȥ��Һ�е��������ӣ������������ӵĻ�ԭ�Լ���������ת��Ϊ�����ӣ�ͨ������pHת��Ϊ�����������������˼��õ�����ͭ��Һ���ݴ˷������
��1����ͭ��ʯ�����������Ӧ��ĽӴ�������ӿ췴Ӧ���ʣ���Ŀ������ߺ�ͭ��ʯ�������ʼ����Ч�ʣ���2�����������۴�����Ϊ0��֪FeCuSi3O6(OH)4����Ԫ�صĻ��ϼ��ǣ�2�ۣ������������Һ�г���Cu2+�⣬�����еĽ�����������Fe2+����3������1�к��ж������裬����NaOH��Һ�����ӷ���ʽΪSiO2+2OH-=SiO32-+H2O����4�����������Ϣ��֪ƯҺ�ļ۸���ã������ѡ�õ��Լ�1������ΪƯҺ��������Լ�ʱ���ݵ��ӵ�ʧ�غ��ԭ���غ��֪������Ӧ�����ӷ���ʽΪClO-+2Fe2++2H+=Cl-+2Fe3++H2O����5���Լ�2��Ϊ�˵���pH���������ӣ��õ�����������ͭ��Һ����˿���ѡ������ͭ��������ͭ����ѡBC������2��һ�����е�����ΪFe(OH)3����6��ͨ�����ӵĸ�����9.632��104C��1.6��10-19C��6.02��1023�����ʵ�����1mol������Cu2����2e����Cu��֪������������������![]() �������ܽ��ͭ��16g��64g/mol��0.25mol��������Һ������ͭ�����ʵ�����0.5mol-0.25mol=0.25mol����Ũ����0.25mol��1L��0.25mol/L��
�������ܽ��ͭ��16g��64g/mol��0.25mol��������Һ������ͭ�����ʵ�����0.5mol-0.25mol=0.25mol����Ũ����0.25mol��1L��0.25mol/L��

 53���ò�ϵ�д�
53���ò�ϵ�д�����Ŀ����1 L��0.01 mol NaAlO2��0.02 mol NaOH����Һ�л���ͨ��CO2����n(CO2)�����Ⱥ���������ͬ�ķ�Ӧ����0.01 mol<n(CO2)![]() 0.015ʱ�����ķ�Ӧ�ǣ�2NaAlO2+ CO2+3H2O=2Al(OH)3��+Na2CO3�����ж�Ӧ��ϵ��ȷ����
0.015ʱ�����ķ�Ӧ�ǣ�2NaAlO2+ CO2+3H2O=2Al(OH)3��+Na2CO3�����ж�Ӧ��ϵ��ȷ����
ѡ�� | n(CO2)/mol | ��Һ�����ӵ����ʵ���Ũ�� |
A | 0 | c(Na+)>c(AlO2-)+c(OH-) |
B | 0.01 | c(Na+)>c(AlO2-)>c(OH-)>c(CO32-) |
C | 0.015 | c(Na+)>c(HCO3-)>c(CO32-)> c(OH-) |
D | 0.03 | c(Na+)>c(HCO3-)> c(OH-)>c(H+) |