题目内容
19.某化学探究小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质的成分.具体操作如下:向C装置中通入一定量的氯气后,测得只生成一种气体Cl2O.可以确定的是C得到的固体中最多含有三种物质,含有氯元素的盐只有一种,且一定含有NaHCO3.现对C中得到的固体进行猜想和验证.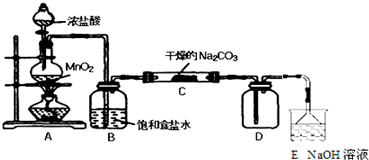
①提出合理猜想:C中一定含有NaHCO3和NaCl;可能含有剩余的Na2CO3.
②设计方案,进行成分检验.请你参与并完成实验步骤3、4以及预期现象和结论,将答案填入下表的相应空格内.限选实验试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、品红、稀盐酸
| 实 验 步 骤 | 预 期 现 象 和 结 论 |
| 步骤1:取C中的少量固体样品于试管中, 加入蒸馏水至固体溶解,然后各取1~2mL 所得溶液分别置于甲、乙两支试管中. | 得到无色溶液. |
| 步骤2:向甲试管中加入过量的BaCl2溶液, 静置. | 若溶液变浑浊,证明固体中含有Na2CO3. |
| 步骤3:取甲试管中上层清液少许于另一只 试管中,滴加少量澄清石灰水, 充分振荡. | 若上层清液变浑浊, 证明固体中含有NaHCO3. |
| 步骤4:向乙试管中先加入过量的稀HNO3 稀HNO3;再滴入少量AgNO3溶液溶液. | 若生成白色沉淀;证明固体中含有氯化钠. |
分析 ①氯气和碳酸钠反应生成碳酸氢钠和氯化钠、氯的氧化物;
②步骤2、碳酸根离子能和氯化钡反应生成碳酸钡沉淀;
步骤3、向溶液中加入澄清石灰水,如果溶液变浑浊,说明含有碳酸氢钠;
步骤4、氯离子和硝酸酸化的硝酸银溶液反应生成氯化银白色沉淀.
解答 解:①氯气和碳酸钠反应中生成氯的氧化物,则氯元素失电子化合价升高,还需要得电子化合价降低,所以还生成NaCl,所以固体中一定含有NaCl,故答案为:NaCl;
故答案为:NaCl;
②步骤2中,加入氯化钡溶液,钡离子和碳酸根离子反应生成碳酸钡白色沉淀,如果溶液变浑浊,说明溶液中含有Na2CO3,
步骤3中,取甲试管中上层清液少许于另一只试管中,滴加少量澄清石灰水,如果上层溶液变浑浊,说明固体中可溶性物质和氢氧化钙发生复分解反应,步骤2中去除碳酸根离子,所以证明固体中含有碳酸氢钠;
步骤4中,先加入过量的稀HNO3,再滴入少量AgNO3溶液,如果产生白色沉淀,则溶液中一定含有氯化钠,
故答案为:
| 步骤2: | Na2CO3 |
| 澄清石灰水 | 上层清液变浑浊 |
| 稀HNO3 AgNO3溶液 | 氯化钠 |
点评 本题采用实验探究的方法考查物质的组成,侧重考查分析、推断能力,明确实验原理是解本题关键,知道常见离子的检验方法,会根据氧化还原反应特点、元素守恒判断生成物,题目难度中等.

练习册系列答案
相关题目
9.把6mol铜粉投入含8mol硝酸和2mol硫酸的稀溶液中,则标准状况下放出的气体的物质的量为( )
| A. | 2 mol | B. | 3 mol | C. | 4 mol | D. | 5 mol |
10.下列反应中有机物被还原的是( )
① +3Fe+6HCl→
+3Fe+6HCl→ +3FeCl3+2H2O
+3FeCl3+2H2O
②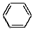 +3H2$→_{△}^{催化剂}$
+3H2$→_{△}^{催化剂}$
③2CH2═CH2+O2→2CH3CHO
④CH3CH2Cl+H2O$→_{△}^{NaOH}$ CH3CH2OH+HCl.
①
 +3Fe+6HCl→
+3Fe+6HCl→ +3FeCl3+2H2O
+3FeCl3+2H2O②
 +3H2$→_{△}^{催化剂}$
+3H2$→_{△}^{催化剂}$
③2CH2═CH2+O2→2CH3CHO
④CH3CH2Cl+H2O$→_{△}^{NaOH}$ CH3CH2OH+HCl.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ③④ |
14. 一氧化碳是一种用途十分广泛的化工基础原料.
一氧化碳是一种用途十分广泛的化工基础原料.
(1)在高温下一氧化碳可将二氧化硫还原为单质硫.已知:
C(s)+O2(g)=CO2(g);△H1=-393.5kJ•mol-1
CO2(g)+C(s)=2CO(g);△H2=+172.5kJ•mol-1
S(s)+O2(g)=SO2(g);△H3=-296.0kJ•mol-1
请写出CO除SO2的热化学方程式2CO(g)+SO2(g)=S(s)+2CO2(g);△H=-270 kJ•mol-1.
(2)工业上一般采用CO与H2在一定条件下反应合成甲醇,反应为:CO(g)+2H2(g)?CH3OH(g).在不同温度下的化学平衡常数(K)如下表:
①某温度下,将2molCO(g)和6molH2(g)充入2L密闭容器中,充分反应后,达到平衡时测得c(CO)=0.5mol/L,则CO(g)的转化率为50%,此时的温度为300℃.
②在恒容条件下,要提高CO(g)的转化率,可以采取的措施有DE(填字母序号).
A、升高温度 B、加入催化剂 C、增加CO(g)的浓度
D、充入H2(g)加压E、分离出甲醇 F、充入稀有气体加压
③实际生产过程中,合成气要进行循环,其目的是提高原料利用率.
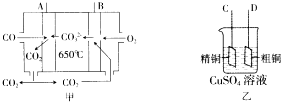
(3)如图甲是--碳酸盐燃料电池,它以CO为燃料,一定比例的Li2CO3和Na2CO3熔融混合物为电解质;图乙是粗铜精炼的装置图,现用燃料电池为电源进行粗铜的精炼实验.
请回答下列问题:
①写出A极发生的电极反应式CO-2e-+CO32-=2CO2.
②要进行粗铜的精炼实验时,则B极应与D极(填“C”或“D”)相连.
③当消耗2.24L(标准状况下) CO时,粗铜电极理论上减少铜的质量小于(填“大于”、“等于”或“小于”)6.4g.
 一氧化碳是一种用途十分广泛的化工基础原料.
一氧化碳是一种用途十分广泛的化工基础原料.(1)在高温下一氧化碳可将二氧化硫还原为单质硫.已知:
C(s)+O2(g)=CO2(g);△H1=-393.5kJ•mol-1
CO2(g)+C(s)=2CO(g);△H2=+172.5kJ•mol-1
S(s)+O2(g)=SO2(g);△H3=-296.0kJ•mol-1
请写出CO除SO2的热化学方程式2CO(g)+SO2(g)=S(s)+2CO2(g);△H=-270 kJ•mol-1.
(2)工业上一般采用CO与H2在一定条件下反应合成甲醇,反应为:CO(g)+2H2(g)?CH3OH(g).在不同温度下的化学平衡常数(K)如下表:
| 温度 | 250℃ | 300℃ | 350℃ |
| A | 2.041 | 0.250 | 0.012 |
②在恒容条件下,要提高CO(g)的转化率,可以采取的措施有DE(填字母序号).
A、升高温度 B、加入催化剂 C、增加CO(g)的浓度
D、充入H2(g)加压E、分离出甲醇 F、充入稀有气体加压
③实际生产过程中,合成气要进行循环,其目的是提高原料利用率.
(3)如图甲是--碳酸盐燃料电池,它以CO为燃料,一定比例的Li2CO3和Na2CO3熔融混合物为电解质;图乙是粗铜精炼的装置图,现用燃料电池为电源进行粗铜的精炼实验.
请回答下列问题:
①写出A极发生的电极反应式CO-2e-+CO32-=2CO2.
②要进行粗铜的精炼实验时,则B极应与D极(填“C”或“D”)相连.
③当消耗2.24L(标准状况下) CO时,粗铜电极理论上减少铜的质量小于(填“大于”、“等于”或“小于”)6.4g.
11.工业上以锂辉石(Li2O-Al2O3-4SiO2,含少量Ca.Mg元素)为原料生产碳酸锂,其部分工艺流程如下:
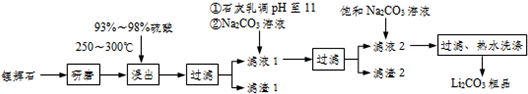
已知:①Li2O•Al2O3•4SiO2+H2SO4(浓)Li2SO4+Al2O3•4SiO2•H2O↓
②不同温度下Li2CO2和Li2OCO4的溶解度如表:
(1)过滤时需要的玻璃仪器有漏斗、玻璃棒、烧杯
(2)滤渣I中分离制取Al2O3,其流程如下图所示(括号中均表示加入过量的试剂):括号内的试剂最好选用D
A.稀盐酸 B.CO2 C.NaOH溶液 D.NHyH2O
滤渣I$→_{I}^{(H+)}$滤液$→_{II}^{()}$滤渣3$→_{Ⅲ}^{灼烧}$Al2O3
步骤Ⅱ中反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+
(3)向滤液Ⅰ中加入石灰水调pH为11的作用是让Mg2+生成Mg(OH)2沉淀,加入Na2CO3溶液的作用是让Ca2+生成 CaCO3沉淀,滤渣2的成分是Mg(OH)2和CaCO3
(4)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失
(5)工业上用电解法将Li2CO3粗品制成高纯LiOH,再向溶液中加入过量NH4HCO3溶液可生成高纯Li2CO3,写出加入NH4HCO3溶液后的反应的化学方程式2LiOH+NH4HCO3=Li2CO3↓+NH3•H2O+H2O.

已知:①Li2O•Al2O3•4SiO2+H2SO4(浓)Li2SO4+Al2O3•4SiO2•H2O↓
②不同温度下Li2CO2和Li2OCO4的溶解度如表:
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2CO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(2)滤渣I中分离制取Al2O3,其流程如下图所示(括号中均表示加入过量的试剂):括号内的试剂最好选用D
A.稀盐酸 B.CO2 C.NaOH溶液 D.NHyH2O
滤渣I$→_{I}^{(H+)}$滤液$→_{II}^{()}$滤渣3$→_{Ⅲ}^{灼烧}$Al2O3
步骤Ⅱ中反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+
(3)向滤液Ⅰ中加入石灰水调pH为11的作用是让Mg2+生成Mg(OH)2沉淀,加入Na2CO3溶液的作用是让Ca2+生成 CaCO3沉淀,滤渣2的成分是Mg(OH)2和CaCO3
(4)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失
(5)工业上用电解法将Li2CO3粗品制成高纯LiOH,再向溶液中加入过量NH4HCO3溶液可生成高纯Li2CO3,写出加入NH4HCO3溶液后的反应的化学方程式2LiOH+NH4HCO3=Li2CO3↓+NH3•H2O+H2O.
9.进行化学实验时必须注意安全,下列选项正确的是( )
| A. |  点燃酒精灯 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上2%~5%的硼酸溶液 | |
| C. |  制备氢气并检验H2的可燃性 | |
| D. | 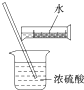 配制硫酸溶液 |
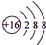 .
. .常温下,D2E2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体.下列说法中正确的是ACD.
.常温下,D2E2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体.下列说法中正确的是ACD.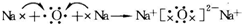 .
. .
.