题目内容
18.等温等压下,等体积的CO2和O3所含分子个数比为1:1,原子个数比为1:1,密度比为11:12.分析 同温同压下,等体积的CO2和O3的物质的量相同,根据m=nM计算质量之比,密度之比等于质量比,结合分子组成分析.
解答 解:同温同压下,等体积的CO2和O3的物质的量相同,设物质的量均为n,
物质的量之比等于分子数之比为1:1;
含原子个数比为n×3×NA:n×3×NA=1:1,
则质量比为44n:48n=11:12,
密度之比等于质量比11:12,
故答案为:1:1;1:1;11:12.
点评 本题考查物质的量的有关计算,把握质量、体积、物质的量、微粒数的关系为解答的关键,侧重分析能力及计算能力的考查,题目难度不大.

练习册系列答案
相关题目
8.如表根据实验操作和现象所得出的结论错误的是( )
| 选 项 | 实验操作 | 实验现象 | 结论 |
| A | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有完全变质 |
| B | 将少量的溴水滴入FeCl2、NaI的混合溶液中,再滴加CCl4,振荡、静置,向上层溶液中滴加KSCN溶液.再向上层溶液中滴加溴水 | 实验现象1: 上层溶液不变红,下层溶液呈紫红色 实验现象2: 上层溶液变红 | 氧化性:Br2>Fe3+>I2 |
| C | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al的 |
| D | 取久置的绿矾(FeSO4•7H2O)溶于水,加入KSCN溶液 | 溶液变为红色 | 绿矾部分或全部被氧化 |
| A. | A | B. | B | C. | C | D. | D |
6.铁、铜混合粉末18.0g加入到100ml 5.0mol/LFeCl3溶液中,剩余固体质量为3.2g.下列说法正确的是( )
| A. | 剩余固体是铁、铜混合物 | |
| B. | 反应后溶液中n (Fe2+)+n(Cu2+)=0.75 mol | |
| C. | 反应后溶液中n (Fe3+)=0.10 mol | |
| D. | 原固体混合物中铜的质量是8.0g |
13.关于配制NaCl溶液的叙述不正确的是( )
| A. | 转移时,要用玻璃棒引流 | |
| B. | 托盘天平称取58.50克食盐,加水配制成1升溶液,NaCl溶液浓度为1mol•L-1 | |
| C. | 溶解食盐的烧杯要洗涤2~3次并将洗涤液转移到容量瓶中 | |
| D. | 搅拌可加速溶解 |
3.下列措施不利于治理雾霾、改善空气质量的是( )
| A. | 推广使用燃煤脱硫技术 | B. | 实施绿化工程 | ||
| C. | 研制开发燃料电池汽车 | D. | 大力发展火电 |
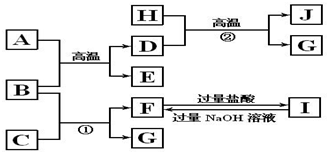
 ,若D最外层只有两个电子,则D的原子结构示意图
,若D最外层只有两个电子,则D的原子结构示意图 ;
;