题目内容
10.如图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料.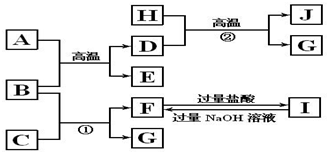
根据图示回答问题:
(1)按要求写出下列化学用语:若B原子中子数比质子数多1,则B的原子符号为2713Al;C的电子式为
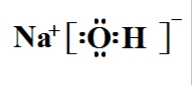 ,若D最外层只有两个电子,则D的原子结构示意图
,若D最外层只有两个电子,则D的原子结构示意图 ;
;(2)写出反应①的化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H↑;写出反应②的化学方程式并标出电子转移的方向和数目

(3)J与稀硝酸反应的离子方程式是3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O;
用排水法收集满该反应的还原产物后,将试管倒扣在水槽中并通入O2使试管刚好全部充满水,假设液体不外溢,则所得溶液的物质的量浓度为$\frac{1}{22.4}$mol/L.
分析 B是地壳中含量最高的金属元素,则B为Al,A、B高温生成E和D,D是单质,则该反应为铝热反应,所以D为Fe,E为Al2O3;H与D在高温下得到G、J,G是气体,J是磁性材料,该转化为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,故H为H2O,J为Fe3O4,G为H2,由反应①Al+C→F+H2,F与酸反应生成I,I与碱反应生成F可知,F为NaAlO2,I为AlCl3,故C为NaOH,据此答题.
解答 解:B是地壳中含量最高的金属元素,则B为Al,A、B高温生成E和D,D是单质,则该反应为铝热反应,所以D为Fe,E为Al2O3;H与D在高温下得到G、J,G是气体,J是磁性材料,该转化为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,故H为H2O,J为Fe3O4,G为H2,由反应①Al+C→F+H2,F与酸反应生成I,I与碱反应生成F可知,F为NaAlO2,I为AlCl3,故C为NaOH,
(1)B为Al,若B原子中子数比质子数多1,则B的原子符号为2713Al,C为NaOH,C的电子式为 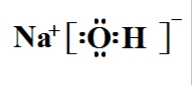 ,D为Fe,是26号元素,D的原子结构示意图是
,D为Fe,是26号元素,D的原子结构示意图是 ,
,
故答案为:2713Al;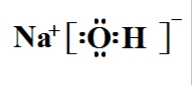 ;
; ;
;
(2)反应①的化学方程式是 2Al+2NaOH+2H2O=2NaAlO2+3H↑;反应②的化学方程式并标出电子转移的方向和数目为 ,
,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H↑; ;
;
(3)J为Fe3O4,J与稀硝酸发生氧化还原反应生成铁离子和一氧化氮,反应的离子方程式是 3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,根据反应4NO+2H2O+O2=4HNO3,设生成的硝酸的物质的量为xmol,则NO气体的体积为22.4xL,即所溶液的体积为22.4xL,所以所得溶液的物质的量浓度为$\frac{x}{22.4x}$mol/L=$\frac{1}{22.4}$mol/L,
故答案为:3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O;$\frac{1}{22.4}$mol/L.
点评 本题以框图形式,考查无机物推断,完成此类题目,关键是找准解题的突破口,再利用顺推法、逆推法相结合进行推断,难度中等.

 一课一练课时达标系列答案
一课一练课时达标系列答案| 实 验 顺 序 | 实 验 内 容 | 实 验 现 象 |
| ① | A+B | 没有现象 |
| ② | B+D | 有气体放出 |
| ③ | B+C | 有沉淀生成 |
| ④ | A+D | 有沉淀生成 |
(2)写出上述实验中的有关化学方程式:
③HCl+AgNO3═AgCl↓+HNO3;
④CaCl2+Na2CO3═2NaCl+CaCO3↓.
| A. | 向豆浆中加入盐卤做豆腐 | |
| B. | 将植物油倒入水中用力搅拌形成油水混合物 | |
| C. | 高压除尘 | |
| D. | 黄河入海口处容易形成三角洲 |
| A. |  三脚架 | B. |  蒸发皿 | C. |  坩埚钳 | D. |  泥三角 |
| A. | a=10、b=9.2 | B. | a<10、b>9.2 | C. | a>10、b=9.2 | D. | a>10、b<9.2 |

 固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ;某科学实验将6mol CO2和8mol H2充入一容积为2L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后的数字表示对应的坐标):回答下列问题:
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ;某科学实验将6mol CO2和8mol H2充入一容积为2L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后的数字表示对应的坐标):回答下列问题: