题目内容
【题目】40℃,向体积为VL的密闭容器中充入NO,容器内各组分的物质的量随时间变化曲线如图所示。下列说法正确的是

A.X是N2O
B.1 min~3 min时,v(NO2)=1/6Vmol·(L·min)-1
C.40℃时该反应的平衡常数为1
D.NO2和X的浓度相等可以作为判断反应到达平衡的标志
【答案】AB
【解析】
根据图像变化,3分钟时反应达到平衡,一氧化氮在减少,二氧化氮和X在增加,则一氧化氮为反应物,二氧化氮与X为生成物,一氧化氮的变化量为3mol,二氧化氮与X为生成物变化量分别为1mol,化学计量系数之比等于参与反应各组分的物质的量的变化量之比,则反应方程式为3NO= NO2+X,根据原子守恒,则X的化学式为N2O。平衡时,NO剩余1mol ,NO2和N2O分别为1mol。
A. 根据上述分析,X是N2O,故A正确;
B. 根据图像分析,1 min~3 min时,二氧化氮物质的量的变化量分别为![]() mol ,v(NO2)=
mol ,v(NO2)=![]() =1/6Vmol·(L·min)-1,故B正确;
=1/6Vmol·(L·min)-1,故B正确;
C. 40℃时该反应的平衡常数为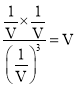 ,故C错误;
,故C错误;
D. 反应进行到任意时刻,NO2和X的浓度都相等,不代表NO2和X的浓度保持不变,不能作为判断反应到达平衡的标志,故D错误;
答案选AB。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目