题目内容
【题目】汽车发动机中生成NO的反应为:![]() ,
,![]() 时该反应的化学平衡常数
时该反应的化学平衡常数![]() 。在
。在![]() 下甲、乙、丙三个恒容密闭容器中,投入
下甲、乙、丙三个恒容密闭容器中,投入![]() 和
和![]() 模拟反应,起始浓度如下表所示。下列判断不正确的是.
模拟反应,起始浓度如下表所示。下列判断不正确的是.
起始浓度 | 甲 | 乙 | 丙 |
|
|
|
|
|
|
|
|
A.起始时,反应速率:丙![]() 甲
甲![]() 乙
乙
B.平衡时,![]() :甲
:甲![]() 丙
丙![]() 乙
乙
C.平衡时,![]() 的转化率:甲
的转化率:甲![]() 乙
乙
D.平衡时,甲中![]()
【答案】B
【解析】
A. 温度相同时,反应物浓度越大,反应速率越快,则起始时,反应速率:丙 ![]() 甲
甲![]() 乙,故A正确;
乙,故A正确;
B. 甲和丙比,反应物浓度按比例增大,相当于增大压强,平衡不移动,但容器体积相同,丙中的气体物质的量多,所以NO浓度大。甲和乙比,甲相等于在乙的基础上增加了N2的浓度,平衡正向移动,NO浓度增大,所以平衡时,![]() :丙
:丙![]() 甲
甲![]() 乙,故B错误;
乙,故B错误;
C. 增大氧气的浓度,平衡正向移动,![]() 的转化率增大,所以平衡时,
的转化率增大,所以平衡时,![]() 的转化率:甲
的转化率:甲![]() 乙,故C正确;
乙,故C正确;
D. 设甲中![]() 反应量为
反应量为![]() ,
,
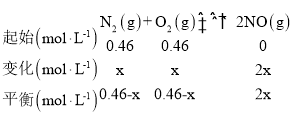
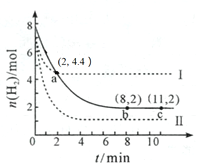
平衡时,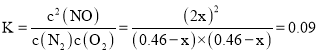 ,解得
,解得![]() ,所以平衡时甲中
,所以平衡时甲中![]()
![]() ,故D正确。
,故D正确。
故选B。

练习册系列答案
相关题目
【题目】探究![]() 反应的速率影响因素,设计了以下实验。下列说法正确的是
反应的速率影响因素,设计了以下实验。下列说法正确的是
锥形瓶标号 |
| 蒸馏水 |
| 反应温度 | 浑浊出现时间 | 备注 |
1 |
| 0 mL | 10 mL |
| 10s | |
2 | 10mL | 5mL | 5 mL |
| 16 s | |
3 | 10mL | 0mL | 10 mL |
| 5 s | 第10s开始浑浊不再增多 |
4 | 10mL | 6mL | 4mL |
| 8s |
A.该反应也可通过测![]() 的体积变化来表示化学反应速率的快慢
的体积变化来表示化学反应速率的快慢
B.3号瓶用![]() 来表示速率为
来表示速率为![]()
C.由2号瓶和3号瓶实验结果可得温度越高反应速率越快
D.由1号瓶和4号瓶实验结果可得温度越高反应速率越快