题目内容
【题目】X、Y、Z、L、M五种元素的原子序数依次增大.X的一种核素没有中子,Y是有机物的主要组成元素,L和M分别是地壳中含量最高的非金属元素和金属元素.回答下列问题:
(1)L的元素符号为;M在元素周期表中的位置为;Z元素的最高正价和最低负价分别为、 , 它的氢化物和最高价氧化物对应水化物反应的化学方程式为 .
(2)Z、X两元素按原子数目比l:3和2:4构成分子A和B,A的电子式为 , B的结构式为 .
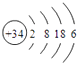
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子原子结构示意图为 .
(4)五种元素的原子半径从大到小的顺序是(用元素符号表示).
(5)羰基硫(COS)分子结构与二氧化碳分子结构相似,所有原子的最外层都满足8电子结构.用电子式表示羰基硫分子: .
(6)写出由X、Z、L三种元素组成的离子化合物与稀NaOH溶液反应的离子方程式: .
【答案】
(1)O;第三周第ⅢA族;+5;﹣3;NH3+HNO3=NH4NO3
(2)![]() ;
;![]()
(3)
(4)Al>C>N>O>H
(5)![]()
(6)NH4++OH﹣=NH3?H2O
【解析】解:X、Y、Z、L、M五种元素的原子序数依次增大.X的一种核素没有中子,则X为H元素;Y是有机物的主要组成元素,则Y为C元素;L和M分别是地壳中含量最高的非金属元素和金属元素,则L为O元素、M为Al,Z的原子序数介于碳、氧之间,则Z为N元素.
(1.)L的元素符号为O;M为Al元素,在元素周期表中的位置为第三周第ⅢA族;Z为N元素,元素的最高正价和最低负价分别为+5、﹣3,它的氢化物和最高价氧化物对应水化物反应的化学方程式为:NH3+HNO3=NH4NO3 , 所以答案是:O;第三周第ⅢA族;+5、﹣3;NH3+HNO3=NH4NO3;
(2.)N、H两元素按原子数目比l:3和2:4构成分子A和B,则A为NH3、B为N2H4 , A的电子式为 ![]() ,B的结构式为
,B的结构式为 ![]() ,所以答案是:
,所以答案是: ![]() ;
; ![]() ;
;
(3.)硒(Se)是人体必需的微量元素,与L(氧)同一主族,Se原子比L(氧)原子多两个电子层,则Se的原子原子结构示意图为: 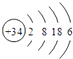 ,所以答案是:
,所以答案是: 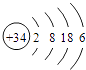 ;
;
(4.)所以元素中H原子半径最小,同周期自左而右原子半径减小,同主族自上而下原子半径增大,故五种元素的原子半径从大到小的顺序是:Al>C>N>O>H,所以答案是:Al>C>N>O>H;(用元素符号表示).
(5.)羰基硫(COS)分子结构与二氧化碳分子结构相似,所有原子的最外层都满足8电子结构,分子中S原子、氧原子与碳原子之间分别形成2对共用电子对,其电子式为: ![]() ,所以答案是:
,所以答案是: ![]() ;
;
(6.)由X、Z、L三种元素组成的离子化合物为NH4NO3等,与稀NaOH溶液反应的离子方程式:NH4++OH﹣=NH3H2O,所以答案是:NH4++OH﹣=NH3H2O.

 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案【题目】甲醇可作为燃料电池的原料。工业上利用CO2和H2在一定条件下反应合成甲醇。
(1)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: 。
(2)甲醇脱氢可制取甲醛CH3OH(g)![]() HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:

①600K时,Y点甲醇的υ(逆) (正)(填“>”或“<”)
②从Y点到X点可采取的措施是____________________________。
③有同学计算得到在t1K时,该反应的平衡常数为8.1mol·L-1。你认为正确吗?请说明理由 。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注。在相同的密闭容器中,使用不同方法制得的Cu2O(Ⅰ)和(Ⅱ)分别进行催化CH3OH的脱氢实验:CH3OH(g)![]() HCHO(g)+H2(g)
HCHO(g)+H2(g)
CH3OH的浓度(mol·L-1)随时间t (min)变化如下表:
序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
可以判断:实验①的前20 min的平均反应速率 ν(H2)= ;实验温度T1 T2(填“>”、“<”);催化剂的催化效率:实验① 实验②(填“>”、“<”)。
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如下图所示装置模拟上述过程, 除去甲醇的离子方程式为 。

【题目】已知常温下浓度为0.lmol/L的下列溶液的pH如下表,下列有关说法正确的是( )
溶质 | NaF | NaClO | Na2CO3 |
pH | 7.5 | 9.7 | 11.6 |
A. 在相同温度下,同浓度的三种酸溶液的导电能力顺序: H2CO3
B. 根据上表,水解方程式ClO-+H2O![]() HClO+OH-的水解常数K=10-7.6
HClO+OH-的水解常数K=10-7.6
C. 若将CO2通入0.lmol/LNa2C03溶液中至溶液中性,则溶液中2c(CO32-)+c(HCO3-)=0.1 mol/L
D. 向上述NaC1O溶液中通HF气体至恰好完全反应时:c(Na+)>c(F-)>(H+)>c(HClO)>c(0H-)
