题目内容
20.某元素的原子最外层电子排布为3s23p2,它的次外层上电子云形状有2种,原子中所有电子占有8个轨道,核外共有14个电子.分析 某元素的基态原子最外层电子排布为3s23p2,应为Si元素,据此解答.
解答 解:某元素的基态原子最外层电子排布为3s23p2,应为Si元素,核外电子排布为1s22s22p63s23p2,它的次外层能级为2s22p6,有s、p两种不同轨道,电子云形状有2种,原子中所有电子占有8个轨道,其中1s、2s共2个轨道,3个2p轨道,2个3p轨道,原子核外共有14个电子,则有14种不同的运动状态,
故答案为:2;8;14.
点评 本题考查原子核外电子排布等知识,侧重于基础知识的考查,为高考高频考点,注意相关基础知识的积累,难度不大.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
10.实验测得在常温下0.1mol•L-1某一元碱(BOH)pH≠13,0.1mol•L-1的某一元酸$\frac{{H}^{+}}{O{H}^{-}}$=1012(HA)溶液中将两种溶液等体积混合后,溶液中离子浓度关系正确的是( )
| A. | [A-]>[B+]>[H+]>[OH-] | B. | [B+]>[A-]>[H+]>[OH-] | C. | [B+]>[A-]>[OH-]=[H+] | D. | [A-]>[B+]>[OH-]>[H+] |
11.常温下,下列各组离子一定可以大量共存的是( )
| A. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-4的溶液中:Na+、SiO32-、SO32-、K+ | |
| B. | 加入Al能放出H2的溶液中:Cl-、Mg2+、NO3-、K+ | |
| C. | 由水电离出的c(OH-)=10-13mol•L-1的溶液中:ClO-、Na+、SO32-、Cl- | |
| D. | pH=1的溶液中:Mg2+、Br-、K+、AlO2- |
15.某化学反应的能量变化如图所示.下列有关叙述正确的是( )
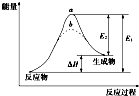

| A. | 逆反应的活化能小于正反应的活化能 | |
| B. | a、b分别对应有催化剂和无催化剂的能量变化 | |
| C. | 该反应的反应热△H=E2-E1 | |
| D. | 催化剂能改变反应的焓变 |
12.设 NA代表阿伏加德罗常数,下列说法中正确的是( )
| A. | 标准状况下,22.4L CO完全燃烧生成CO2分子数为NA | |
| B. | 17g 氨气所含电子数为NA | |
| C. | 在常温、常压下,11.2L氯气所含的原子数目为NA | |
| D. | 32g氧气所含的原子数目为NA |
 .
.