题目内容
一定条件下,有如下反应:
2CO (g) + O2(g)=2CO2(g) ΔH1=" -" 566.0kJ·mol-1
3Fe(s) +2O2(g)=Fe3O4 (s) ΔH2=-1118.3kJ·mol-1
Fe3O4(s)+4CO(g) 3Fe(s) +4CO2 (g) ΔH3
3Fe(s) +4CO2 (g) ΔH3
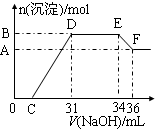
(1)试计算,ΔH3 =
(2)已知1100℃时,反应Fe3O4(s)+4CO(g) 3Fe(s)+4CO2 (g) ΔH3的化学平衡常数为4.8×10-3。若在1100℃时,测得高炉中c(CO2)=0.020mol·L-1,c(CO)=0.10mol·L-1,此时该反应 (填“是”或“否”)处于平衡状态,理由是 ,此时υ正 υ逆(填“>”、“<”或“=”)。
3Fe(s)+4CO2 (g) ΔH3的化学平衡常数为4.8×10-3。若在1100℃时,测得高炉中c(CO2)=0.020mol·L-1,c(CO)=0.10mol·L-1,此时该反应 (填“是”或“否”)处于平衡状态,理由是 ,此时υ正 υ逆(填“>”、“<”或“=”)。
(3)下列试剂可以用于吸收工业尾气中的CO2的是 。
a.(NH4)2CO3溶液 b.氨水 c.NaHSO3溶液 d.CaCl2溶液
(1)—13.7 kJ?mol?1 (2分)
(2)否(1分)该条件下 c4(CO2)/c4(CO)=0.0016 < 4.8×10-3,所以不处于平衡状态。(3分)
> (1分)
(3)ab (2分)
解析试题分析:(1)根据盖斯定律,ΔH3 =2ΔH1—ΔH2=—13.7 kJ?mol?1。
(2)由高炉中c(CO2)=0.020mol·L-1,c(CO)=0.10mol·L-1,求出Q= c4(CO2)/c4(CO)=(0.020mol·L-1)4÷(0.10mol·L-1)4=0.0016 < 4.8×10-3,所以不处于平衡状态;浓度商Q小于平衡常数,说明平衡正向移动,所以υ正> υ逆。
(3)a、(NH4)2CO3能与CO2、H2O反应生成NH4HCO3,可以吸收CO2,正确;b、NH3、H2O与CO2反应生成(NH4)2CO3或NH4HCO3,可以吸收CO2,正确;c、NaHSO3不与CO2反应,不能吸收CO2,错误;d、CaCl2不与CO2反应,不能吸收CO2,错误。
考点:本题考查盖斯定律、平衡状态的判断、反应速率的判断、工业尾气的处理。



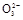
 2I-+S4
2I-+S4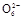 ),共用去V mL硫代硫酸钠溶液。
),共用去V mL硫代硫酸钠溶液。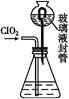
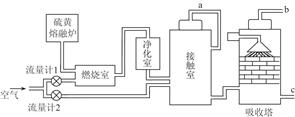
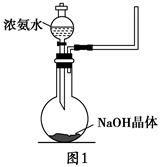
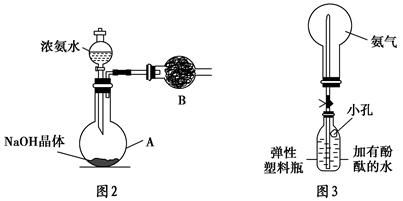
 NH4++OH-,NaOH晶体使该可逆反应的平衡向左移动
NH4++OH-,NaOH晶体使该可逆反应的平衡向左移动