��Ŀ����
ʵ���о����֣����ᷢ��������ԭ��Ӧʱ�������Ũ��Խϡ����Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�͡�ijͬѧȡһ���������Ͻ���100mLijŨ�ȵ������ַ�Ӧ����Ӧ������������ų����ڷ�Ӧ���������Һ�У���μ���4mol��L��1������������Һ����������������Һ�����(mL)������ij��������ʵ���(mol)�Ĺ�ϵ��ͼ��ʾ��C>0����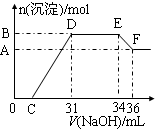
�Իش��������⣺
��1��д����Ӧ������DE�ε����ӷ�Ӧ����ʽ�� ��EF�����ɺ���Ԫ�����ӵ������� ��
��2���Ͻ�����������Ϊ g ��
��3��C��ֵΪ mL��
��4��������Һ�����ʵ���Ũ��Ϊ mol��L��1
��1��NH4��+OH��=NH3?H2O ƫ����������ǻ����������1�֣�
��2��1.344 ��3��7 ��4��1.48
���������������1��D��Eһ�γ�������û�з����仯��ΪNH4NO3��NaOH��Ӧ����Ӧ�����ӷ���ʽΪNH4��+OH��=NH3��H2O��EF��Ϊ�������������������Ƶķ�Ӧ����Al(OH)3 +OH��=AlO2��+2H2O��Al(OH)3 +OH��=[Al(OH)4]�������EF�����ɺ���Ԫ�����ӵ�������ƫ����������ǻ����������
��2��DE����������������Һ�������34ml��31ml��3mol������вμӷ�Ӧ����������Ϊ0.003L��4mol/L��0.012mol�����Ը��ݷ�ӦNH4��+OH��=NH3?H2O��֪��NH4�������ʵ�����0.012mol�����ݵ�ԭ���غ��֪�����ɰ��������ʵ�����0.012mol�������ǻ�ԭ������Ը��ݵ��ӵ�ʧ�غ��֪���������ʵ�������0.012mol��8��0.008mol��3����3��0.024mol���������������0.024mol��56g/mol��1.344g��
��3�����ݷ�ӦʽFe3����3OH��=Fe(OH)3����Al3����3OH��=Al(OH)3����֪��C��D�������������Ƶ����ʵ�����0.024mol��3��0.008mol��3��0.096mol���������0.096mol��4mol/L��0.024L��24ml������C���Ӧ�������31ml��24ml��7ml��
��4��E���Ӧ�������������ƣ������������غ��֪�������Ƶ����ʵ�����0.034L��4mol/L��0.136mol�����Ը��ݵ�ԭ���غ��֪��ԭ��������ʵ�����0.136mol��0.012mol��0.148mol�����������Ũ����0.148mol��0.1L��1.48mol��L��1��
���㣺�������������ķ�Ӧ���йؼ��㡣

��ѧ������ũҵ�����о�����Ҫ�����ã���ϵ��ũҵ�����Ƿ���ա���ѧ������ũҵ�����еĹ㷺Ӧ�ã�Ϊ��ѧ���ϵĴ��ģ��ҵ�����ṩ����̨��
��1���ںϳɰ����豸(�ϳ���)�У������Ƚ�������Ŀ����______________��
��2����������Ĺ����г������һЩ���������һ��ɲ����������ַ���������
��Һ���շ���NO��NO2��2NaOH=2NaNO2��H2O
����ԭ����8NH3��6NO2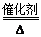 7N2��12H2O(NOҲ�����Ƶķ�Ӧ)
7N2��12H2O(NOҲ�����Ƶķ�Ӧ)
�����ɫ��ѧ�ĽǶȷ������ַ��������ӣ�____________________��
��3��ij���ʳ���NH3�Ʊ�NH4NO3����֪����NH3��NO�IJ�����96%��NO��HNO3�IJ�����92%������HNO3����ȥ��NH3������ռ�ܺ���NH3����(�������������)��________%��
��4���������һ�ֳ��õĵ��ʣ��������ʹ�øû���ʱ����Ӧע���������������±�(������Ӧע���������ɼ���)��
| | ע������ | ���� |
| �� | ______________ | ____________ |
| �� | ________________ | ____________ |
��������;ʮ�ֹ㷺�������ھ�ˮ�����������⣬�������������ᡢ��ȡ�
��1����ҵ�Ͽ���������ʯ����Ϊԭ������Ư�ۣ�Ư�۵���Ч�ɷ��� ��
��2����ҵ�������뵼����Ϲ���������£�
��д���Ʊ��ֹ�ʱ��Ӧ�Ļ�ѧ����ʽ�� ��
�ڴֹ���������Ӧ��õ��е�ϵ͵�Һ̬���Ȼ����г�����һЩ�߷е㡢�ѻӷ���Һ̬���ʣ�������з����ᴿ�����ᴿ����Ϊ ������ĸ����
| A������ | B������ | C����ȡ | D���ᾧ |
 3Fe(s) +4CO2 (g) ��H3
3Fe(s) +4CO2 (g) ��H3 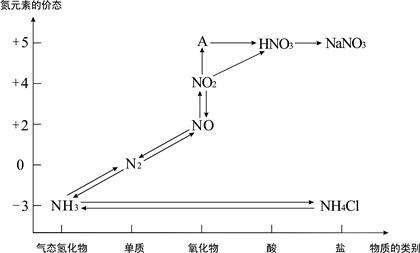
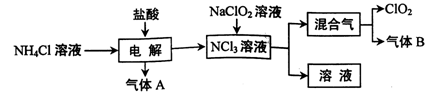
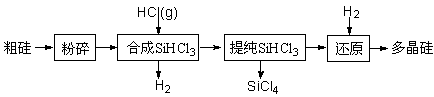
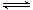 Si (s) + 3HCl (g) ��H ��0����ƽ�ⳣ������ʽΪK = ��Ϊ���ԭʱSiHCl3��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�� ��
Si (s) + 3HCl (g) ��H ��0����ƽ�ⳣ������ʽΪK = ��Ϊ���ԭʱSiHCl3��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�� ��