题目内容
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 在标准状况下,11.2L O2和22.4L NO混合并充分反应后得到的气体的分子数为NA
B. 常温下0.1mol·L-1NH4NO3溶液中的氮原子数为0.2NA
C. 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA
D. 25℃时,1.0L pH=13的Ba(OH)2溶液中,含有的OH-数目为0.2NA
【答案】C
【解析】
A项,11.2L O2和22.4L NO混合恰好反应生成22.4LNO2,即1molNO2,但由于存在2NO2![]() N2O4的反应,因此得到气体分子数小于NA;B项,未注明溶液体积,无法计算溶液中含有的氮原子数;C项,1 mol Na与足量O2反应,无论生成Na2O还是Na2O2,Na都是由0价变为+1价,所以转移电子数为NA;D项,25 ℃时,1.0 L pH=13的Ba(OH)2溶液中,n(OH-)=1.0L×
N2O4的反应,因此得到气体分子数小于NA;B项,未注明溶液体积,无法计算溶液中含有的氮原子数;C项,1 mol Na与足量O2反应,无论生成Na2O还是Na2O2,Na都是由0价变为+1价,所以转移电子数为NA;D项,25 ℃时,1.0 L pH=13的Ba(OH)2溶液中,n(OH-)=1.0L×![]() mol/L=0.1mol,所以含有的OH-数目为0.1NA。
mol/L=0.1mol,所以含有的OH-数目为0.1NA。
A项,11.2L O2和22.4L NO混合恰好反应生成22.4LNO2,即1molNO2,但由于存在2NO2![]() N2O4的反应,分子数小于NA,故A项错误;
N2O4的反应,分子数小于NA,故A项错误;
B项,未注明溶液体积,无法计算溶液中含有的氮原子数,故B项错误;
C项,1 mol Na与足量O2反应,无论生成Na2O还是Na2O2,Na都是由0价变为+1价,所以转移电子数为NA,故C正确;
D项,25 ℃时,1.0 L pH=13的Ba(OH)2溶液中,n(OH-)=1.0L×![]() mol/L=0.1mol,所以含有的OH-数目为0.1NA,故D项错误。
mol/L=0.1mol,所以含有的OH-数目为0.1NA,故D项错误。
综上所述,本题正确答案为C。

【题目】以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工。
(1)将水蒸气通过红热的炭即可产生水煤气。反应为C(s)+H2O(g)CO(g)+H2(g) ΔH=+131.3 kJ·mol-1。
①该反应在常温下_______(填“能”或“不能”)自发进行。
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是____(填字母,下同)。
a.容器中的压强不变
b.1 mol H—H键断裂的同时,断裂2 mol H—O键
c.c(CO)=c(H2)
d.密闭容器的容积不再改变
(2)将不同量的CO(g)和H2O(g)分别通入体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g)CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 2 | 4 | 1.6 | 2.4 | 6 |
2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
①实验1中从反应开始至平衡以CO2表示的平均反应速率为v(CO2)=________(取小数点后两位,下同)。
②该反应的正反应为________(
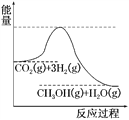
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2,达到平衡后下列措施中能使c(CH3OH)增大的是________。
a.升高温度
b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1 mol CO2和3 mol H2