题目内容
【题目】中学化学中几种常见物质的转化关系如下图所示
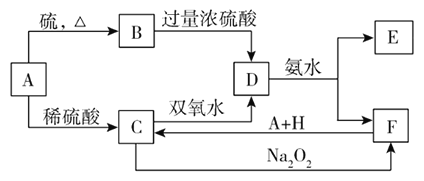
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体.请回答下列问题:
(1)红褐色胶体中F粒子直径大小的范围:________.
(2)A、B、H的化学式:A__________、B__________、 H________.
(3)①H2O2分子的电子式为______________。
②写出C的酸性溶液与双氧水反应的离子方程式: _______________________。
(4)写出鉴定E中阳离子的实验方法和现象:_______________________。
(5)在C溶液中加入与C等物质的量的Na 2 O 2 ,恰好使C转化为F,写出该反应的离子方程式:____________________________。
【答案】 1-100nm Fe FeS H2SO4 ![]() 2Fe2++H2O2+2H+=2Fe3+2H2O 取少量E于试管中,用胶头滴管滴加适量的氢氧化钠溶液,加热试管,若生成使湿润的红色石蕊试纸变蓝的气体,则证明铵根离子的存在 4Fe2++4Na2O2+6H2O= 4Fe(OH)3(胶体) +O2↑+8Na+
2Fe2++H2O2+2H+=2Fe3+2H2O 取少量E于试管中,用胶头滴管滴加适量的氢氧化钠溶液,加热试管,若生成使湿润的红色石蕊试纸变蓝的气体,则证明铵根离子的存在 4Fe2++4Na2O2+6H2O= 4Fe(OH)3(胶体) +O2↑+8Na+
【解析】将D溶液滴入沸水中可得到以F为分散质的红褐色胶体,说明F为Fe(OH)3,D溶液中含有Fe3+,D是由B和过量浓硫酸反应生成的,所以D是Fe2(SO4)3,因此E为(NH4)2SO4,C与双氧水反应生成Fe2(SO4)3,所以C为FeSO4,因此A是单质铁,A与硫反应生成FeS,所以B是FeS。在转化关系F+H+A=C中,因F是Fe(OH)3、A是Fe、C是FeSO4,根据元素守恒得H是硫酸。
(1)、红褐色胶体中F是Fe(OH)3,因胶体的粒子直径在1-100nm之间,所以答案是:1-100nm。
(2)根据上述分析可知,A是Fe、B是FeS,H是H2SO4。
(3)、①.双氧水是共价化合物,O与H之间、O与O之间均以共价键相连,所以双氧水的电子式是:![]() 。
。
②.C为FeSO4,与双氧水反应时,C作还原剂,双氧水作氧化剂,其反应的离子方程式是:2Fe2++H2O2+2H+=2Fe3+2H2O。
(4)因E为(NH4)2SO4,常采用与碱共热检验生成的气体是否为氨气来检验铵根离子,所以其检验方法是:取少量E于试管中,用胶头滴管滴加适量的氢氧化钠溶液,加热试管,若生成使湿润的红色石蕊试纸变蓝的气体,则证明铵根离子的存在。
(5)、在C(FeSO4)溶液中加入与C(FeSO4)等物质的量的Na 2 O 2 ,恰好使C(FeSO4)转化为F(Fe(OH)3),根据得失电子守恒和原子守恒规律,其反应的离子方程式是:4Fe2++4Na2O2+6H2O= 4Fe(OH)3(胶体) +O2↑+8Na+。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案