题目内容
有一种纸质软电池,该电池采用薄层纸片作为载体和传导体,一面附着锌,另一面附着二氧化锰。电池总反应为Zn+2MnO2+H2O=ZnO+2MnO(OH),关于此电池,下列说法正确的是
| A.该电池Zn为负极,ZnO为正极,MnO2催化剂] |
| B.该电池的正极反应为MnO2+e-+H2O=MnO(OH)+OH- |
| C.放电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn |
| D.电池工作时OH-通过薄层纸片向附着二氧化锰的电极移动 |
B
试题分析:A、反应中Zn被氧化,应为原电池的负极,MnO2被还原,应为原电池的正极,错误;B、从总反应式可知MnO2被还原为MnO(OH),故电池的正极反应式为MnO2 + e– + H2O=" MnO(OH)" + OH–,正确;C、放电时外电路电子由Zn流向MnO2,内电路依靠离子的定向移动导电,错误;D、电池工作时OH–向负极(Zn电极)移动,错误。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
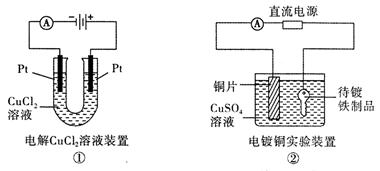
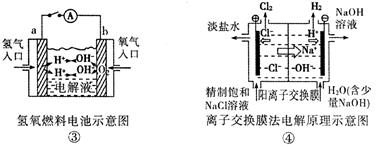
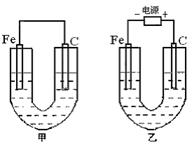
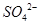 从右向左移动。下列分析正确的是
从右向左移动。下列分析正确的是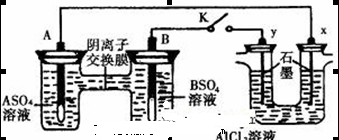
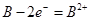
 Cl2↑+H2↑
Cl2↑+H2↑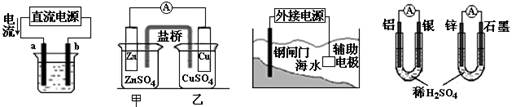
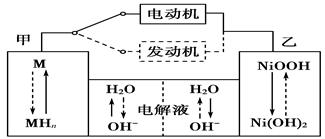
 2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,甲电
2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,甲电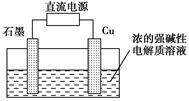
 Cu2O+H2↑,阴极的电极反应式是_____________________。
Cu2O+H2↑,阴极的电极反应式是_____________________。