题目内容
某小组为研究电化学原理,设计如图装置。下列叙述不正确的是( )
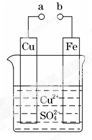

| A.a 和 b 不连接时,铁片上会有金属铜析出 |
| B.a 和 b 用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu |
| C.无论 a 和 b 是否连接,铁片均会溶解,溶液均从蓝色逐渐变 成浅绿色 |
| D.a 和 b 分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 |
D
试题分析:A.金属性:Fe>Cu,所以发生:Fe+Cu2+= Fe2++Cu。正确。B.该装置为原电池,铁作负极,铜作正极,电子由铁经导线流向Cu电极,在Cu电极上发生反应:Cu2++2e-=Cu。正确。C.通过A、B的分析发现:无论 a 和 b 是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色。正确。D.a 和 b 分别连接直流电源正、负极,该装置为电解池,a 是阳极, b是阴极。Cu2+向负电荷多的铁电极方向移动。错误。

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目


 2PbSO4(s)+2H2O(l),下列说法错误的是
2PbSO4(s)+2H2O(l),下列说法错误的是