题目内容
【题目】在酸性溶液中能大量共存的离子组是( )
A. K+、NO3-、Cu2+ B. K+、OH﹣、Na+
C. Ba2+、SO42-、Na+ D. Ca2+、CO32-、Na+
【答案】A
【解析】
该溶液中一定存在大量的氢离子,
A.K+、NO3-、Cu2+之间不发生反应,也不与氢离子反应,在溶液中能够大量共存,故A正确;
B. OH﹣与H+反应生成水,不能大量共存,故B错误;
C. Ba2+与SO42-反应生成硫酸钡沉淀,不能大量共存,故C错误;
D. Ca2+与CO32-反应生成碳酸钙沉淀,不能大量共存,故D错误;
综上所述,本题选A。

【题目】同学们用下图所示实验,探究SO2及其水溶液的性质。下列说法正确的是
|
|
|
ⅰ. SO2溶于水 | ⅱ. 向ⅰ的水溶液中滴入品红溶液 | ⅲ.将ⅱ的溶液加热 |
A. ⅰ的溶液呈酸性,是由于SO2+H2O![]() H2SO3
H2SO3![]() 2H++SO32-
2H++SO32-
B. ⅱ中品红褪色,不足以证明具有漂白性的是SO2
C. ⅲ中溶液恢复红色,一定是H2SO3分解造成的
D. 上述实验涉及SO2的溶解性和强氧化性
【题目】“C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-49.0kJ/mol。相关数据如下:
CH3OH(g)+H2O(g) △H=-49.0kJ/mol。相关数据如下:
容器 | 甲 | 乙 |
反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
平衡时c(CH3OH) | c1 | c2 |
平衡时能量变化 | 放出29.4kJ | 吸收akJ |
请回答:
①c1_____c2(填“>”、“<”或“=”);a=__________。
②若甲中反应10s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是__________mol/(L·s)。
(2)压强为P1时,向体积为1L的密闭容器中充入bmol CO和2bmol H2,CO和氢气发生反应CO(g)+2H2(g)![]() CH3OH(g)。平衡时CO的转化率与温度、压强的关系如图所示。请回答:
CH3OH(g)。平衡时CO的转化率与温度、压强的关系如图所示。请回答:
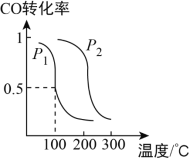
①该反应属于__________(填“吸”或“放”)热反应;P1__________P2(填“>”、“<”或“=”)。
②100℃时,该反应的平衡常数K=__________(用含b的代数式表示)。
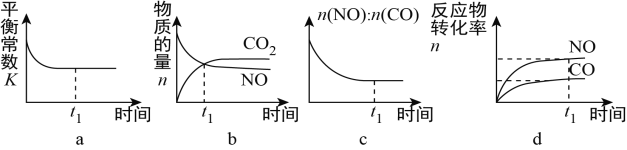
(3)治理汽车尾气的反应是2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) △H<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=1:2的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是__________(选填字母)。
2CO2(g)+N2(g) △H<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=1:2的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是__________(选填字母)。