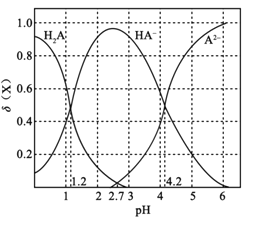
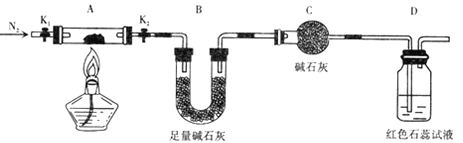
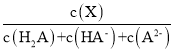题目内容
【题目】设NA为阿伏加德罗常数的值,下列有关说法正确的是
A.常温常压下,1.8g甲基(—CD3)中含有的电子数为NA
B.0. lmol环氧乙烷(![]() )中含有的共价键数为0. 3 NA
)中含有的共价键数为0. 3 NA
C.常温下,1L pH=9的CH3COONa溶液中,发生电离的水分子数为1×10-9 NA
D.加热条件下,含0.2molH2SO4的浓硫酸与足量铜反应,转移电子数小于0.2NA
【答案】D
【解析】
A.—CD3的相对质量为12+2×3=18,含电子数为6+3=9,所以1.8g即0.1mol该甲基中含有的电子数为0.9NA,故A错误;
B.一个环氧乙烷分子中共价键数目为7,所以0.1mol环氧乙烷含有的共价键数目为0.7NA,故B错误;
C.常温下,pH=9的CH3COONa溶液中,c(OH-)=10-5mol/L,且全部由水电离,所以发生电离的水分子为10-5mol/L×1L=10-5mol,故C错误;
D.浓硫酸在与铜反应过程中变稀,稀硫酸与铜不反应,所以含0.2molH2SO4的浓硫酸与足量铜反应,转移电子数小于0.2NA,故D正确;
故答案为D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目