题目内容
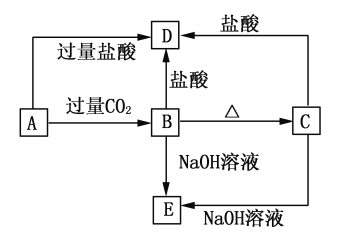
【题目】A、B、C、D、E五种化合物中均含有地壳中含量最多的金属元素,它们的转化关系如图所示,其中A为澄清溶液,B、C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
(1)写出化学式:A________,B________,C________,D________,E________。
(2)写出下列反应的离子方程式:
A→B:_____________________
A→D:_____________________
【答案】(1)KAlO2 Al(OH)3 Al2O3 AlCl3 NaAlO2(每空1分)
(2)AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
AlO2-+4H+=Al3++2H2O(每空2分)
【解析】
试题分析:B、C都既能与盐酸反应又能与NaOH溶液反应,应为两性化合物,因B加热分解可生成C,则可知B为Al(OH)3,C为A12O3,则D为AlCl3,E为NaAlO2,若取A溶液灼烧,焰色反应为紫色(透过蓝色钴玻璃片),说明A中含有K元素,A能与二氧化碳反应生成Al(OH)3,则A应为KAlO2,
(1)通过以上分析知,A、B、C、D、E分别是KAlO2、Al(OH)3、A12O3、AlCl3、NaAlO2;
(2)A→B的反应为AlO2-和Al(OH)3的转化,反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
A→D的反应为AlO2-和Al3+的转化,反应的离子方程式为AlO2-+4H+=Al3++2H2O。

【题目】一定温度下,在三个体积均为1.0 L的恒容密闭容器中,充入一定量的H2和SO2发生下列反应:3 H2(g) + SO2(g)![]() 2 H2O(g) + H2S(g),下列说法正确的是( )
2 H2O(g) + H2S(g),下列说法正确的是( )
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
H2 | SO2 | H2 | SO2 | ||
容器Ⅰ | 300 | 0.3 | 0.1 | 0.02 | |
容器Ⅱ | 300 | 0.6 | 0.2 | ||
容器Ⅲ | 240 | 0.3 | 0.1 | 0.01 | |
A.该反应正反应为吸热反应
B.容器Ⅲ达到平衡的时间比容器I短
C.240℃时,该反应的平衡常数为1.08×104
D.容器Ⅱ达到平衡时SO2的转化率比容器I小