题目内容
【题目】研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出。在反应结束后的溶液中,逐滴加入4 mol·L-1NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。下列说法不正确的是( )
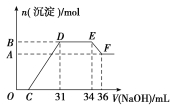
A.OC段离子反应方程式为:H++OH-===H2O
B.溶液中n(NH![]() )=0.012 mol
)=0.012 mol
C.溶液中结合OH-能力最强的离子是H+,最弱的离子是Al3+
D.欲测定F点沉淀的质量,实验步骤是:过滤、洗涤、干燥、称量
【答案】
【解析】选C。根据题意,加入NaOH溶液,没有产生气体,说明还原产物为NH![]() ,溶液中含有的离子是Al3+、Fe3+、H+、NH
,溶液中含有的离子是Al3+、Fe3+、H+、NH![]() 。向该溶液中加入NaOH溶液,开始没有析出沉淀,因此结合OH-的能力由强到弱的顺序是H+、Fe3+、Al3+、NH
。向该溶液中加入NaOH溶液,开始没有析出沉淀,因此结合OH-的能力由强到弱的顺序是H+、Fe3+、Al3+、NH![]() ,然后是Al(OH)3沉淀的溶解。A.根据图像可知在OC段发生的反应为剩余的硝酸与NaOH溶液反应,离子方程式是H++OH-===H2O,正确;B.根据图可知在DE段反应消耗NaOH溶液的体积是3 mL,根据NH
,然后是Al(OH)3沉淀的溶解。A.根据图像可知在OC段发生的反应为剩余的硝酸与NaOH溶液反应,离子方程式是H++OH-===H2O,正确;B.根据图可知在DE段反应消耗NaOH溶液的体积是3 mL,根据NH![]() +OH-===NH3·H2O可知:n(NH
+OH-===NH3·H2O可知:n(NH![]() )=n(OH-)=cV=4 mol/L×0.003 L=0.012 mol,正确;C.根据反应的先后顺序可知结合OH-最强的离子是H+,最弱的离子是NH
)=n(OH-)=cV=4 mol/L×0.003 L=0.012 mol,正确;C.根据反应的先后顺序可知结合OH-最强的离子是H+,最弱的离子是NH![]() ,错误;D.欲测定F点沉淀的质量,应该将互不相溶的固体与液体分离,并洗涤,洗去附着在沉淀表面的杂质离子,然后干燥再称重,故实验步骤是:过滤、洗涤、干燥、称量,正确。
,错误;D.欲测定F点沉淀的质量,应该将互不相溶的固体与液体分离,并洗涤,洗去附着在沉淀表面的杂质离子,然后干燥再称重,故实验步骤是:过滤、洗涤、干燥、称量,正确。

【题目】向甲溶液中加入(或通入)乙溶液(或气体),生成的沉淀的量与加入的乙的量的关系符合如图的是
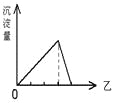
选项 | A | B | C | D |
甲 | Al2(SO4)3 | NaAlO2 | AlCl3 | Ca(OH)2 |
乙 | NH3 | HCl | NaOH | CO2 |
A. A B. B C. C D. D
【题目】下列关于有机物因果关系的叙述中,完全正确的一组是( )
选项 | 原因 | 结论 |
A | 乙烯和苯都能使溴水褪色 | 苯分子和乙烯分子含有相同的碳碳双键 |
B | 乙酸分子中含有羧基 | 可与NaHCO3溶液反应生成CO2 |
C | 纤维素和淀粉的化学式均为(C6H10O5)n | 它们互为同分异构体 |
D | 乙酸乙酯和乙烯在一定条件下都能与水反应 | 二者属于同一反应类型 |
A. A B. B C. C D. D