题目内容
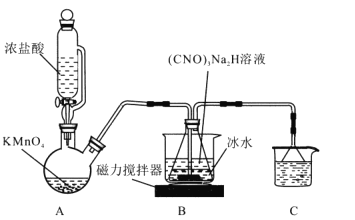
【题目】实验室制取少量溴乙烷的装置如右图所示。
根据题意完成下列填空:
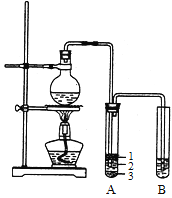
(1)圆底烧瓶中加入的反应物是溴化钠、_____和1:1的硫酸。配制体积比1:1的硫酸所用的定量仪器为_________(选填编号)。
a.天平 b.量筒 c.容量瓶 d.滴定管
(2)写出加热时烧瓶中发生的主要反应的化学方程式__________________________。
(3)将生成物导入盛有冰水混合物的试管A中,冰水混合物的作用是_______________。试管A中的物质分为三层(如图所示),产物在第____层。
(4)试管A中除了产物和水之外,还可能存在_____、________(写出化学式)。
(5)用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的正确方法是_____(选填编号)。
a.蒸馏 b.氢氧化钠溶液洗涤
c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的物质的名称是______________。
(6)实验员老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是:_______________。
【答案】乙醇 b NaBr+H2SO4→HBr+NaHSO4 CH3CH2OH+HBr![]() CH3CH2Br+H2O 冷却、液封溴乙烷 3 HBr CH3CH2OH d 乙烯 反应会产生Br2,腐蚀橡胶
CH3CH2Br+H2O 冷却、液封溴乙烷 3 HBr CH3CH2OH d 乙烯 反应会产生Br2,腐蚀橡胶
【解析】
(1)制备溴乙烷需乙醇和溴化氢反应,故需要加乙醇;配制稀硫酸需要量筒来量所需浓硫酸的体积,故选b;
(2)溴化钠和浓硫酸反应先制得溴化氢,溴化氢再和乙醇反应生成溴乙烷;
(3)冰水将溴乙烷冷凝;
(4)还可能有挥发出来的溴化氢和乙醇;
(5)有机物呈棕黄色是因为溶有溴单质,有强氧化性,可以和亚硫酸钠反应而除去;氢氧化钠虽然和溴单质能反应,但和溴乙烷也发生反应,故选d;在浓硫酸做催化剂的作用下乙醇发生消去反应生成乙烯,注意名称应该写汉字;
(6)考虑橡胶管换成玻璃管,原因是溴腐蚀橡胶。

 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案