题目内容
【题目】国内某科技研究小组首次提出一种新型的Li+电池体系,该体系征集采用含有I-、Li+的水溶液,负极采用固体有机聚合物,电解质溶液采用LiNO3溶液,聚合物离子交换膜作为隔膜将液态正极和固态负极分隔开(原理示意图如图)。已知:I-+I2=I3-,则下列有关判断正确的是
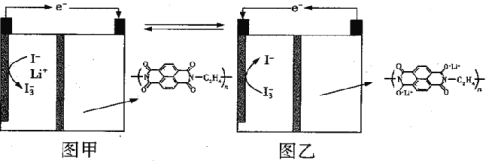
A. 图甲是原电池工作原理图,图乙是电池充电原理图
B. 放电时,正极液态电解质溶液的颜色变浅
C. 充电时,Li+从右向左通过聚合物离子交换膜
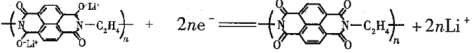
D. 放电时,负极的电极反应式为:
【答案】B
【解析】
题目已知负极采用固体有机聚合物,甲图是电子传向固体有机聚合物,图甲是电池充电原理图,则图乙是原电池工作原理图,放电时,负极的电极反应式为: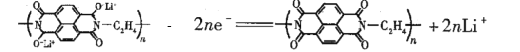
正极的电极反应式为:I3-+2e-= 3I-。
A. 甲图是电子传向固体有机聚合物,电子传向负极材料,则图甲是电池充电原理图,图乙是原电池工作原理图,A项错误;
B. 放电时,正极液态电解质溶液的I2也会的得电子生成I-,故电解质溶液的颜色变浅,B项正确;
C. 充电时,Li+向阴极移动,Li+从左向右通过聚合物离子交换膜,C项错误;
D. 放电时,负极是失电子的,故负极的电极反应式为:

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
【题目】某学生探究0.25mol/LAl2(SO4)3溶液与0.5mol/LNa2CO3溶液的反应,实验如下。
实验1 |
|
实验2 |
|
下列分析正确的是( )
A. 实验1中,白色沉淀a是Al2(CO3)3
B. 实验2中,白色沉淀b一定是Al2(OH)2(CO3)2
C. 检验白色沉淀a、b是否洗涤干净,均可用盐酸酸化的BaCl2溶液
D. 实验1、2中,白色沉淀成分不同的原因与混合后溶液的pH无关