题目内容
(6分)过氧化钙是一种安全无毒的氧化物,通常含有部分CaO,且带有数量不等的结晶水。为分析某过氧化钙样品的组成,进行了如下实验。
① 称取0.270 g样品,灼热使之完全分解,生成CaO、O2和H2O,得到的O2在标准状况下体积为33.6 mL。
② 另取0.120 g样品,溶于稀盐酸,加热煮沸,使生成的H2O2完全分解。然后将溶液中的Ca2+ 完全转化为CaC2O4沉淀,经过滤洗涤后,将沉淀溶于热的稀硫酸,用0.0200 mol·L-1 KMnO4溶液滴定,共用去31.0 mL KMnO4溶液。化学方程式如下:
5CaC2O4+2KMnO4+8H2SO4 = K2SO4+2MnSO4+5CaSO4+10CO2↑+8H2O
(1) 写出CaO2受热分解的化学方程式。
(2) 计算样品中CaO2的质量分数。
(3) 计算样品中CaO2·x H2O的x值。
【答案】
(1) 2CaO2 = 2CaO+O2↑ (1分)
(2) w (CaO2)=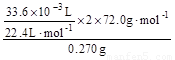 ×100%=80%
(2分)
×100%=80%
(2分)
(3) n (CaC2O4)=n (Ca2+)=31.0×10-3 L×0.0200 mol·L-1×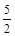 =0.00155 mol
=0.00155 mol
其中CaO2所含的n (Ca2+)=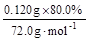 =0.00133 mol
=0.00133 mol
m (CaO)=(0.00155 mol-0.00133 mol)×56.0 g·mol-1 =0.012 g
m (H2O)=0.120 g―0.120g ×80.0%―0.012 g=0.012 g
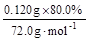 ∶
∶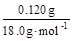 =2∶1 x=
=2∶1 x=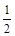 (3分)
(3分)
【解析】

练习册系列答案
相关题目